
科目: 来源: 题型:
小明同学在学习“硫酸及其盐的某些性质与用途”的过程中,进行如下实验探究。
[实验一]探究浓硫酸的氧化性,将实验室常用的药品放入如图所示的实验装置后,加热装置甲。(夹持和加热装置省略)
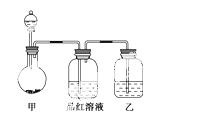
(1)该装置设计上存在明显缺陷,请指出:_______________________________。
(2)写出装置甲中反应的化学方程式:______________________________
__________________。装置乙中的试剂是:_______________________。
[实验二]探究某硫酸亚铁盐固体是否变质
(3)请你帮助小明同学完成如下实验方案:
| 实验操作 | 预期现象和结论 |
查看答案和解析>>
科目: 来源: 题型:
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩 擦剂中氢氧化铝的定性检验。
擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是
___________________________________________________________________________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是_________
___________________________________________________________________________。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3
沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
___________________________________________________________________________。
(4)C中反应生成BaCO3的化学方程式是__________________________________________
___________________________________________________________________________。
(5)下列各项措施中,不能提高测定准确度的是________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
查看答案和解析>>
科目: 来源: 题型:
实验室以含有Ca2+、Mg2+、Cl-、SO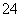 、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
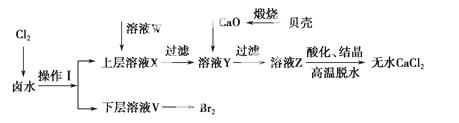
(1)操作Ⅰ使用的试剂是________,所用主要仪器的 名称是________。
名称是________。
(2)加入溶液W的目的是________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是________。酸化溶液Z时,使用的试剂为________。
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1. |
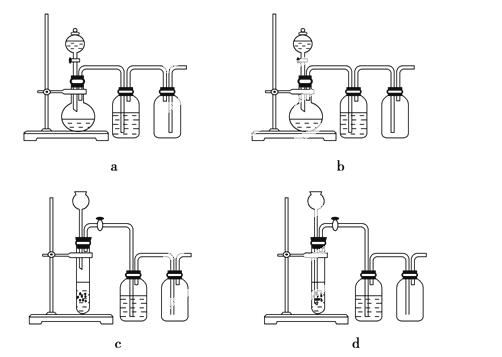
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是________。
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3酸性强于H2CO3;将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于________。设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论)。
____________________________。仪器自选。供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
查看答案和解析>>
科目: 来源: 题型:
油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝的食品添加剂,逐步转换为无铝的食品添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)和碳酸氢铵(臭粉)组成。为测定试样中小苏打的质量分数ω(NaHCO3),实验小组同学设计了如下装置进行实验。

实验过程:
①按上图组装仪器,检查装置的气密性;
②将试样m1 g放入硬质玻璃管中,装置B、C、D中药品如上 图,已知加药品后装置B的质量为m2 g、装置C的质量为m3 g;
图,已知加药品后装置B的质量为m2 g、装置C的质量为m3 g;
③关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4 g、装置C的质量为m5 g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)装置B的作用为
________________________________________________________________________;
装置C的作用为
________________________________________________________________________。
(3)实验过程中通入N2的目的为
________________________________________________________________________。
(4)用下列各项所提供的数据能计算出ω(NaHCO3)的是________(填选项字母)。
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的ω(NaHCO3),若能,写出ω(NaHCO3)的计算式。
________(填“能”或“不能”),________(若不能,此空不作答)。
查看答案和解析>>
科目: 来源: 题型:
菠菜营养丰富,素有“蔬菜之王”之称,是一种高效的补铁剂。长期以来民间流传“菠菜不能与豆腐同食”、“菠菜根比菠菜茎和叶更有营养”等说法。某学校化学兴趣小组的同学拟通过实验探究以下问题:
①菠菜是否含有丰富的铁?
②菠菜是否含有草酸类物质?
③菠菜根中铁的含量是否比菠菜茎和叶中的高?
通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,其中草酸钙不溶于水。
他们设计的实验步骤如下:
Ⅰ.
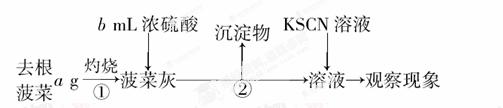
Ⅱ.取菠菜根a g,使用相同仪器、试剂,重复I中实验,观察实验现象。
Ⅲ.将菠菜在少量开水中煮沸2~3 min,冷却后滤去菠菜,得滤液。向滤液中加入足量Ca(OH)2溶液,然后再加入足量试剂X,观察现象。
请回答以下问题:
(1)操作①中使用的仪器除三脚架、酒精灯、玻璃棒外还需要________,操作②的名称是________。
(2)可以说明菠菜根中Fe元素含量要比菠菜茎和叶中多的现象是________。
(3)菠菜中的Fe是+2价还是+3价?________。
(4)通过步骤Ⅲ可以确定菠菜中含有草酸类物质。由于滤液中含有CO32-,故需加入试剂X排除CO32-的干扰。则X是________(写化学式),加入试剂X后观察到的现象是________。
查看答案和解析>>
科目: 来源: 题型:
某品牌消毒液包装说明的部分内容摘录如下:主要有效成分为次氯酸钠,有效氯含量8000 mg/L~10000 mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用,切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉处保存。请完成以下实验探究过程:
(一)阅读材料,获取信息
(1)推测该消毒液的酸碱性:________,原因是(用离子方程式表示)________。
(2)该消毒液还具有的化学性质是________性和________性。
(3)从该消毒液的保存要求分析,导致其失效的外界因素主要是________。
(二)确定要研究的问题
该消毒液对碳钢制品是否有腐蚀作用?
(三)实验探究
用烧杯取少量样品,将一颗光亮的铁钉放入烧杯中浸泡一段时间,对可能产生的现象有如下假设:假设①:有明显现象;假设②:无明显现象。
(4)基于假设①,结论是铁钉被腐蚀,预期的实验现象是________。
(5)基于假设②,结论是________,请设计实验进一步验证该结论,叙述实验操作:
________。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是________。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag。
【设计实验方案,验证假设】
(2)甲同学从上述实验的生成物中检验出Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:
________________________________________________________________________。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容
(提示:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① | |
| ② | |
| …… | 若银镜消失,假设2成立。 |
| 若银镜不消失,假设2不成立。 |
【思考与交流】
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3-都氧化了Ag。
你是否同意丙同学的结论,并简述理由:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的离子方程式:
________________________________________________________________________,
________________________________________________________________________。
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)
①用蒸馏水完全溶解CaCl2后,加入
________________________________________________________________________。
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-。
③加入__________________________________________________________________,使沉淀完全溶解。
④_______________________________________________________________________,
得到纯净的硝酸钙晶体。
查看答案和解析>>
科目: 来源: 题型:
下列实验方案可行的是( )
A.检验溶液中是否有SO42-时,加入BaCl2溶液,再加稀硝酸,观察沉淀是否消失
B.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
C.选用25 mL碱式滴定管量取14.80 mL 1 mol·L-1 NaOH溶液
D.检验溶液中是否含有CO32-时,加入稀盐酸,将产生的气体通入澄清石灰水
查看答案和解析>>
科目: 来源: 题型:
中学化学教材中有大量数据,下列是某同学对数据的利用情况,其中正确的是( )
A.利用焓变的数据或熵变的数据一定都能单独判断反应是否能自发进行
B.利用沸点数据推测将一些液体混合物分离开来的可能性
C.利用反应热数据的大小判断不同反应的反应速率的大小
D.利用溶液的pH与7的大小关系,来判断任何温度下溶液的酸碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com