
科目: 来源: 题型:
下列物质分类正确的是 ( )
A.Cu(OH)2难溶于水,属于非电解质
B.SO2能与碱反应生成盐和水,属于酸性氧化物
C.NH4Cl组成中不含金属离子,不属于盐
D.HCl气体溶于水电离成H+和Cl-,属于离子化合物
查看答案和解析>>
科目: 来源: 题型:
分类是化学研究中常用的方法.下列分类方法中,不正确的是 ( )
A.依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等
B.依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还 原反应
原反应
C.依据能量的变化,将化学反应分为放热反应和吸热反应
D.依据组成元素的种类,将纯净物分为单质和化合物
查看答案和解析>>
科目: 来源: 题型:
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%-103.0%)的主要流程如下:
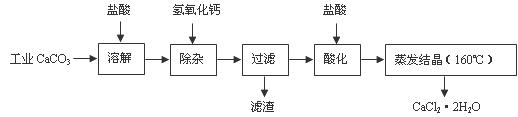
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0-8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的试验操作是 。
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①
;② 。
(3)测定样品中Cl- 含量的方法是:a.称取0.7500 g样品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用0.05000 mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。
①计算上述样品中CaCl2·2H2O的质量分数为 。
②若用上述办法测定的样品中CaCl2·2H2O的质量分数有时超过100.0%(测定过程中产生的误差可忽略),其可能原因有
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:

该实验的主要操作步骤如下:
①配制100 mL 1.0 mol·L-1的盐酸溶液;
②用________(填仪器名称并注明规格)量取7.5mL 1.0 mol·L-1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100 mL 1.0 mol·L-1的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母) 。
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤②_______________ 步骤③___________
(3)实验步骤⑤中应选用__________(填字母)的量筒。
A.100 mL B.200 mL C.500 mL
(4)读数时除恢复到室温外,还要注意
①______________________________,②_________________________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____L/mol。
查看答案和解析>>
科目: 来源: 题型:
氯碱工业是最基本的化学工业之一,其主要原理基于电解饱和食盐水:2NaCl+2H2O 2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
(1)电解前,如果粗盐中SO42- 含量较高,必须添加钡试剂除去SO42- ,该钡试剂可以是______________(填字母代号)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(2)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
利用盐泥生产MgSO4·7H2O晶体的工艺流程如下图所示。
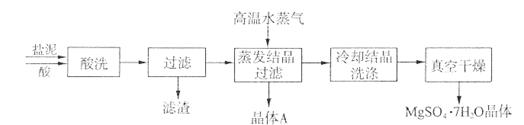
回答下列问题:
①酸洗过程中加入适量硫酸控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,CaCO3在此过程中转化为CaSO4,请解释此转化得以发生的原因 。
②过滤所得滤渣的主要成分为 。
③根据下图分析,蒸发结晶过滤所得晶体A主要成分为 。
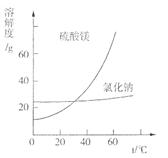
④真空干燥MgSO4·7H2O晶体的原因是 。
(3)已知NaCl在60 ℃的溶解度为37.1 g,现电解60 ℃精制饱和食盐水1371 g,经分析,电解后溶液密度为1.37 g·cm-3,其中含有20 g NaCl,则电解后NaOH的物质的量浓度为________________mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
I. 下面列出了几组物质或粒子,请将合适的组号填写在空格上。
①金刚石与“足球烯”(C60)
②CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
③235U、238U ④氧气(O2)与臭氧(O3)
⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3) ⑥淀粉和纤维素
⑦ 
(1)是同素异形体的是 ,(填序号,下同)
(2)是同位素的是 ,
(3)是同分异构体的是 ,
(4)是同一物质的是 。
II. 下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤C2H6 ⑥MgF2 ⑦HNO3
(1)只由离子键构成的物质是______________(填序号,下同)(2)由离子键和非极性键构成的物质是______________(3)由极性键和非极性键构成的物质是______________
III. 提纯下列物质(括号内的物质是杂质),请将所选用的除杂试剂和分离方法(填字母或者序号)填入对应的空格中(若不选,填“无”)
除杂试剂:A. 盐酸 B. 酸性高锰酸钾 C. 氢氧化钠溶液 D. (浓)溴水
E. H2(催化剂) F. CaO G. NaCl
分离方法:① 蒸馏 ② 分液 ③ 洗气 ④ 过滤
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| (1) | 酒精(水) | ||
| (2) | 乙烷(乙烯) | ||
| (3) | 硬脂酸钠溶液(甘油) | ||
| (4) | 苯(苯酚) | ||
| (5) | SiO2(Al2O3) |
查看答案和解析>>
科目: 来源: 题型:
在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为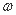 ,物质的量浓度为c mol·L-1。则下列选项不正确的是
,物质的量浓度为c mol·L-1。则下列选项不正确的是
A.溶质的质量分数为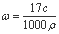
B.用水稀释该溶液,OH- 的物质的量增加
C.该溶液中共有6种微粒
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5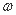
查看答案和解析>>
科目: 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)<M(乙),则气体的压强:甲>乙
B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
C.若M(甲)>M(乙),则气体体积:甲<乙
D.若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目: 来源: 题型:
下述实验不能达到预期实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 将2.5 g CuSO4·5H2O溶解在97.5 g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 | 检验NaHCO3固体中是否含Na2CO3 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
查看答案和解析>>
科目: 来源: 题型:
下列说法或表达正确的是
①次氯酸的结构式为 H—Cl—O
②含有离子键的化合物都是离子化合物
③蛋白质、漂白粉、苛性钾、液氨分别为纯净物、混合物、强电解质和非电解质
④丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应
⑤酸性氧化物不一定是非金属氧化物,但是碱性氧化物一定是金属氧化物
A.①②④ B.①③⑤ C.②④⑤ D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com