
科目: 来源: 题型:
一定条件下,通过下列反应可实现燃煤
烟气中硫的回收:SO2(g)+2CO(g)  2CO2(g)+S(l) ΔH<0若反应在恒容的密闭容器中进行,下列有关说法正
2CO2(g)+S(l) ΔH<0若反应在恒容的密闭容器中进行,下列有关说法正
确的是 ( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应的平衡常数不变
查看答案和解析>>
科目: 来源: 题型:
COCl2(g)  CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入
惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是 ( )
A.①② ④ B.①④⑥ C.②③⑤ D.③⑤⑥
④ B.①④⑥ C.②③⑤ D.③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
一定条件下反应2AB(g) A2(g)+B2(g)达到平衡
A2(g)+B2(g)达到平衡
状态的标志是
A.单位时间内生成nmolA2,同时消耗2n molAB
B.容器内三种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目: 来源: 题型:
一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)  Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是 ( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是 ( )
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
科目: 来源: 题型:
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5的酸碱性为 ,试样的pH值 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)=H2O(g)  H= -241.8KJ/mol
H= -241.8KJ/mol
C(s)+1/2O2(g)=CO(g)  H= -110.5KJ/mol
H= -110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式 ;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 ;
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g)
2NO(g)  H>0
H>0
若1mol空 气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol.计算该温度下的平衡常数K= ___________;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是
气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol.计算该温度下的平衡常数K= ___________;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是  。
。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g)已知该反应的 H>
H> 0,简述该设想能否实现的依据 。
0,简述该设想能否实现的依据 。
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
氯气在298  K、100 kPa
K、100 kPa 时,在1 L水中可溶解0.09 mol,实验
时,在1 L水中可溶解0.09 mol,实验 测得
测得
溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为________;
(2)估算该反应的平衡常数________(列式计算);i
(3)在上述平衡体系中加入少量NaOH固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将________(填“增大”、“减小”或
“不变”),平衡将向________移动。
查看答案和解析>>
科目: 来源: 题型:
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g) 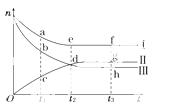
 2NH3(g),500 K、30 MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示
2NH3(g),500 K、30 MPa下n(NH3)、n(H2)和n(N2)随时间变化的关系如图所示
请回答下列问题:
(1)上图中属于氢气物质的量随时间变化的曲线是______(填“Ⅰ”、“Ⅱ”或 “Ⅲ”).
(2)关于t2时刻的说法正确的是________.
A.t2时该反应达到平衡状态
B.t2时Ⅱ和Ⅲ代表的物质反应速率相同
C.t2时氢气、氮气与氨气的反应速率之比为3∶1∶2
D.t2时氨气与氢气的物质的量相同
(3)对于Ⅱ所代表的物质,其逆反应速率最大的点是________(填“c”、“d”或“g”);对于Ⅰ所代表的物质,其正反应速率最小的点是________(填“a”、“e”或“f”).
(4)其他条件不变,只改变温度,在改变的这个温度下反应至t3时刻,此时n(H2)比图象中的值大,那么该温度最可能的是________.
A.673 K B.273 K
C.373 K D.1073 K
查看答案和解析>>
科目: 来源: 题型:
在2 L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,
2NO2(g)体系中, n(NO)随时间的变化如表:
n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=__________.已知:K300℃>K350℃,则该反应是________热反应.
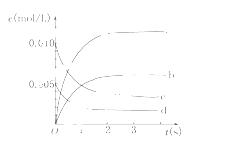
(2)图中表示NO2的变化的曲线是________.用O2表示从0~2 s内该反应的平均速率v=________.

(3)能说明该反应已达到平衡状态的是________.
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________.
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效催化剂
查看答案和解析>>
科目: 来源: 题型:
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体
2G(g)。忽略固体体
积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
| 压强/MPa
温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
①b<f ②915℃、2.0MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
查看答案和解析>>
科目: 来源: 题型:
反应X(g)+Y(g) 2Z(g);
2Z(g);
 H<0,达到平衡时,下列说法正确的是
H<0,达到平衡时,下列说法正确的是
A.减小容器体积,平衡向右移动 B.加入催化剂,Z的产率增大
C.增大c(X),X的转化率增大 D.降低温度,Y的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com