
科目: 来源: 题型:
已知化学反应A2(g) + B2(g) = 2AB(g)的能量变化如图所示,
判断下列叙述中正确的是
A.每生成2分子AB吸收b kJ热量
B.该反应热△H=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1molA—A和1molB—B键,放出a kJ能量
查看答案和解析>>
科目: 来源: 题型:
某反应A + B = C + D 在低温下不能自发进行,在高温下能自发进行,对该反应过程△H、
△S的判断正确的是
A.△H <0 △S >0 B.△H >0 △S >0
 C.△H <0 △S <0 D.△H >0 △S <0
C.△H <0 △S <0 D.△H >0 △S <0
查看答案和解析>>
科目: 来源: 题型:
下列有关说法中正确的是
A.合成氨中采用及时分离氨气提高反应物的转化率
B.升高温度能使吸热反应速率加快,使放热反应速率减慢
C.增大压强,化学反应速率一定加快,平衡一定发生移动
D.工业上电解饱和食盐水的阴极反应:2Cl--2e-===Cl2↑
查看答案和解析>>
科目: 来源: 题型:
某小组取一定质量的FeSO4固体,利用下图装置进行实验。250mL容量瓶
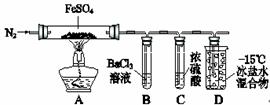
| 实验过程 | 实验现象 | |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。
(1)实验③反应的离子方程式是 。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______气体,依据是 。
(3)实验④反应的离子方程式是__ _____。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)___ __ (填“正确”或“不正确”)理由
。
查看答案和解析>>
科目: 来源: 题型:
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为
Mg(OH)2
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 实验结论 |
| 实验Ⅰ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | ①气体成分为 |
| 实验Ⅱ | ②取实验Ⅰ中的白色不溶物,洗涤,加入足量 | ③ 产生气泡沉淀全部溶解 | 白色不溶物可能含有MgCO3 |
| 实验Ⅲ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | ④溶液中存在 |
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示:
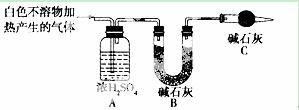
称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因: 。
查看答案和解析>>
科目: 来源: 题型:
某氧化铁样品中含有少量的FeCl2杂质.现要测定其中铁元素的质量分数,按以下步骤进行实验:
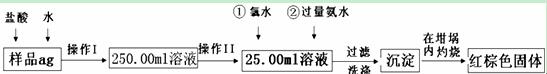
请根据图的流程,回答下列问题:
(1)操作I所用到玻璃仪器除烧杯、玻璃棒、胶头滴管以外,还必须有 ;
(填仪器名称)操作II必须用到的仪器是 。(填字母)
A.50ml烧杯 B.50ml量筒 C.100ml量筒 D.25ml滴定管
⑵再加入氨水的离子方程式为 。
⑶检验沉淀是否洗涤干净的操作是 。
⑷将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质
量为b2g,若b1—b2=0.3,则接下来还应进行的操作是
。
⑸若坩埚的质量为W1g,坩埚与加热后固体的总质量为W2g,则样品中铁元素的质量分数
是 。
⑹有学生认为上述实验步骤太繁琐,他认为,将样品溶于水后充分搅拌,在空气中加热蒸干
燃烧称量即可,请你评价是否可行? 。(填“可行”或“不可行”)
查看答案和解析>>
科目: 来源: 题型:
下图表示某气态单质A及其化合物之间的转化关系 (某些产物和反应条件已略去)。
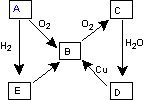 (1)A单质的电子式
(1)A单质的电子式
(2)写出E生成B的化学方程式:
。
(3)①写出由D生成B的离子方程式 。
②常温下D和E恰好完全反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是 。
查看答案和解析>>
科目: 来源: 题型:
2.8gFe全部溶于一定浓度200mLHNO3溶液中,得到标准状况下气体1.12L,测得反应后溶液pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是( )
A.反应后溶液中铁元素一定只以Fe3+形式存在 B.1.12L气体可能是NO、NO2的混合气体
C.反应后溶液中c(NO3-)=0.85mol/L D.反应后的溶液最多还能溶解1.82gFe
查看答案和解析>>
科目: 来源: 题型:
现将35g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2L(标准状况),其质量为19.6g,则过剩的锌粉的质量为( )
A.1.0g B.2.0g C.2.5g D.3.5g
查看答案和解析>>
科目: 来源: 题型:
下列关于SiO2和CO2的说法中正确的是( )
A.CO2、SiO2分别是碳酸和硅酸的酸酐 B.CO2和SiO2与水反应分别生成相应的酸
C.CO2是酸性氧化物,SiO2是两性氧化物 D.CO2和SiO2都是由相应的分子组成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com