
科目: 来源: 题型:
由黄铜矿(主要成分是CuFeS2) 炼制精铜的工艺流程示意图如下:
炼制精铜的工艺流程示意图如下:
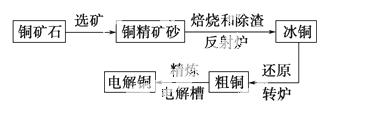
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1 000 ℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是____________________、__________________________,反射炉内生成 炉渣的主要成分是________;
炉渣的主要成分是________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1 200 ℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____________;
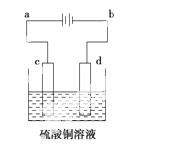
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为____________________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________________。
查看答案和解析>>
科目: 来源: 题型:
合成氨的流程示意图如下:
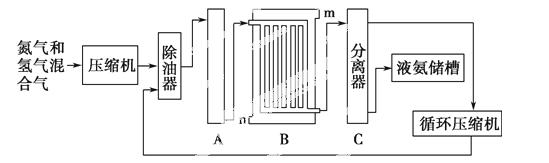
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是________、________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学方程式_______________________。
(2)设备A中含有电加热器,触媒和热交换器,设备A的名称是________,其中发生的化学反应方程式为____________。
(3)设备B的名称为________,其中m和n是两个通水口,入水口是________(填“m”或“n”)。不宜从相反方向通水的原因是______________。
(4)设备C的作用是______________________。
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
已知1 000 K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于________。
查看答案和解析>>
科目: 来源: 题型:
合成氨工业、硫酸工业的生产工艺 流程如图所示 。
。

合成塔和接触室中的反应分别为
N2(g)+3H2(g) 2NH3(g) ΔH<0;
2SO2(g)+O2(g) 2SO3(g) ΔH<0。
(1)写出流程中设备的名称:B________,X________。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是___________________。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是________(填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是_______________。
(5)工业生产中常用氨-酸法进行尾气脱硫,以达到消 除污染、
除污染、 废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是___________________。
(6)根据化学 平衡移动原理,下列条件或措施合理的是________(填序号)。
平衡移动原理,下列条件或措施合理的是________(填序号)。
①合成氨工业在高压下进行
②合成氨工业和硫酸工业都使用催化剂
③及时将氨液化而分离
④硫酸工业中,净化后的炉气中要有过量空气
⑤合成氨工业和硫酸工业都采用适宜的温度
查看答案和解析>>
科目: 来源: 题型:
海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
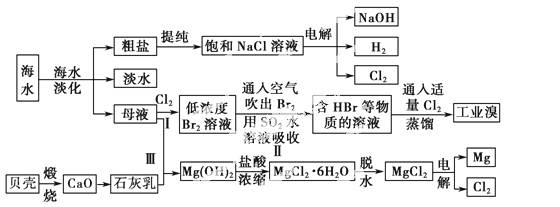
(1)在粗盐中含有Ca2+、Mg2+、SO等杂质,电解精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是____________(填编号)。
(2)工业上电解饱和食盐水的离子方程式:_________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是____________ _____。
_____。
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_____________________。
(4)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入________溶液,充分搅拌后经________(填操作方法)可得纯 净的Mg(OH)2。
净的Mg(OH)2。
(5)在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2·6H2O的原因:______________________。
(6)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________(填序号)。
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
查看答案和解析>>
科目: 来源: 题型:
石油和煤炭加工过程涉及多种技术和设备。
(1)石油分馏时,在不断向____________(填工业设备名称)内投放原料的同时获得产品,该过程为____________操作过程。
(2)石油裂化分为热裂化、________和加氢裂化,裂化的目的是提高________的产量。
(3)煤的洗选是为了降低原煤中灰分和________的含量。煤的流化床燃烧是指空气从底部吹向煤炭颗粒,并使全部煤炭颗粒________进行燃烧的过程。
(4)煤的直接液化是煤与适当溶剂混合后在高温和________存在下与________________作用生成液体燃料的过程。
查看答案和解析>>
科目: 来源: 题型:
由于工业发 展,燃烧设备不断增多,设备规模不断增大。这些工厂排放的烟气中都会有大量的
展,燃烧设备不断增多,设备规模不断增大。这些工厂排放的烟气中都会有大量的 SO2废气。据统计,我国1995年工业SO2的排放量为1 396万吨,2006年工业SO2的排放量达到了3 800万吨,由于SO2的污染,我国每年损失高达1 100亿元。
SO2废气。据统计,我国1995年工业SO2的排放量为1 396万吨,2006年工业SO2的排放量达到了3 800万吨,由于SO2的污染,我国每年损失高达1 100亿元。
(1)写出两个工业生产过程中产生SO2的实例:
①________________________________________________________________________、
②________________________________________________________________________。
(2)防治SO2污染可采用的措施有(写出三种):
①________________________________________________________________________、
②________________________________________________________________________、
③___________________ _____________________________________________________。
_____________________________________________________。
(3)湿式石灰石—石膏法脱硫工艺是烟气脱硫技术中最成熟的一种方法。其工艺流程是:烟气经锅炉预热器出来,进入电除尘器除掉大部分粉煤灰烟尘,再经过一个专门的热交换器,然后进入吸收塔,烟气中的SO2与含有石灰石的浆液进行气 液接触,通入空气后生成石膏(CaSO4·2H2O),经脱硫的烟气,应用循环气体加热器进行再加热,进入烟囱,排入大气。
液接触,通入空气后生成石膏(CaSO4·2H2O),经脱硫的烟气,应用循环气体加热器进行再加热,进入烟囱,排入大气。
①写出湿法石灰石—石膏法脱硫所涉及的化学反应方程式:
________________________________________________________________________
________________________________________________________________________。
②用石灰石浆液作SO2吸收剂而不用熟石灰吸收SO2的原因是:________________________________________________________________________
_____________ ___________________________________________________________。
___________________________________________________________。
③上述过程中得到的石膏,如果含氯化合物(主要来源于燃料煤)超过杂质极限值,则石膏产品性能变坏。工业上消除可溶性氯化物的方法是__________________。
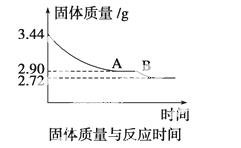
(4)某化学兴趣小组为了测定烟气脱硫所得石膏的组成(CaSO4·xH2O)即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如下图所示。数据表明当固体的质量为2.72 g后不再改变。求:
①石膏的化学式。②图像中AB段对应化合物的化学式。
查看答案和解析>>
科目: 来源: 题型:
电石浆是氯碱工业中的一种废弃物,其大致组成如下表所示:
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其他不溶于酸的物质 |
| 质量分数 (%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程:
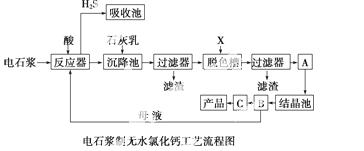
已知氯化钙晶体的化学式是CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中加入的酸应选用 ________。
(2)脱色槽中应加入的物质X是______________;设备A的作用是______________;设备B的名称为 ______________;设备C的作用是 ____________。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是________。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是__________________________
______________________。
查看答案和解析>>
科目: 来源: 题型:
某工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料)。
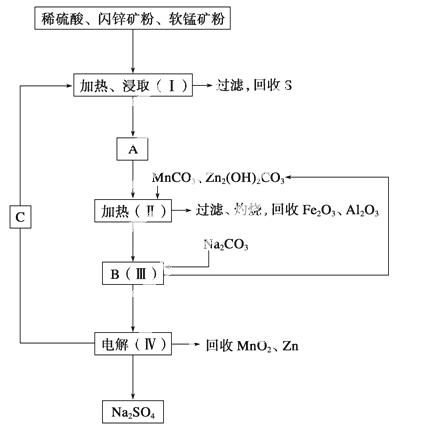
已知:①A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②Ⅳ中电解方程式为MnSO4+ZnSO4+2H2OMnO2+Zn+2H2SO4。
(1)A中属于还原产物的是______ ____。
____。
(2)加入MnCO3、Zn2(OH)2CO3的作用是_____________________________________
________________________________________________________________________。
Ⅱ需要加热的原因是____________________________________________________。
C的化学式是________________________。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是________。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是________。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需进行的操作有蒸发浓缩、________、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是________。
查看答案和解析>>
科目: 来源: 题型:
工业上生产硫酸的流程图如下:

请回答下列问题:
(1)早期生产硫酸以黄铁矿为原料,但现在工厂生产硫酸以硫黄为原料,理由是________________________________________________________________________。
(2)在气体进入催化反应室前需净化的原因是_________________________ ________
________
_____________________ ___________________________________________________。
___________________________________________________。
(3)在催化反应室中通常使用常压,在此条件下SO2的转化率为90%。但是部分发达国家采取高压条件下制取SO3,采取加压措施的目的除了加快反应速率外,还可以____________________________,从而提高生产效率。
(4)工业生产中常用氨—酸法进行尾气脱硫,以达到消除污染,废物利用的目的。用化学方程式表示其反应原理:____________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)除硫酸工业外,还有许多工业生产。下列相关的工业生产流程中正确的是________。
A.海水提溴:海水浓缩热空气或水蒸气溴蒸气碱液吸收液溴
B.海水提镁:海滩贝壳石灰水MgO熔化电解镁
C.工业制硝酸:空气NO2水吸收硝酸—→尾气处理
D.工业合成氨:天然气一定条件下氢气合成塔过量氮气NH3、H2、N2水冷分离氨
查看答案和解析>>
科目: 来源: 题型:
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。请回答下列问题:
(1)目前,以下“技术”中,可用于“海水淡化”的是___________________________
(填序号)。
①蒸馏法 ②膜分离法(电渗析、反渗透) ③冷冻法 ④离子交换法
(2)海 水晒盐利用的化学原理是____________________________________________;
水晒盐利用的化学原理是____________________________________________;
分离食盐晶体后的母液中含有____________,经过分离、提纯后,可用于_________。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应的 离子方程式为________________________________________________________________________;
离子方程式为________________________________________________________________________;
电解所用的食盐水需要精制,其原因是_____________________________________
________________________________________________________________________;
精制时所用试剂:盐酸、BaCl2溶液、NaOH溶液、Na2CO3溶液,加入试剂时,Na2CO3溶液必须在加入__________________________________________________________之后加入。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫的废气同时回收二氧化硫的方法,该方法的流程如下:
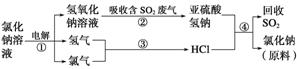
写出反应②、④的化学方程式:_____________________________________________、
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com