
科目: 来源: 题型:
下列有关溶液组成的描述合理的是
A.无色溶液中可能大量存在Al3+、NH4+、Cl‾、S2‾
B.酸性溶液中可能大量存在Na+、ClO‾、SO42‾、I‾
C.弱碱性溶液中可能大量存在Na+、K+、Cl‾、HCO3‾
D.中性溶液中可能大量存在Fe3+、K+、Cl‾、SO42‾
查看答案和解析>>
科目: 来源: 题型:
水溶液中能大量共存的一组离子是
A.Na+、Ca2+、Cl-、SO42-
B.Fe2+、H+ 、SO32-、ClO-
C.Mg2+、NH4+、Cl- 、SO42-
D.K+、Fe3+、NO3-、SCN-
查看答案和解析>>
科目: 来源: 题型:
某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子。以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4·7H2O)和汞的方案。
【药品】 NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
【实验方案】
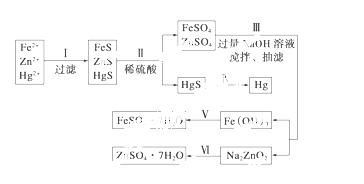
【问题探究】
(1)步骤Ⅱ所发生反应的离子方程式为__________________________________。
(2)步骤Ⅲ中抽滤的目的是____________,该步骤产生Fe(OH)3的反应的离子方程式为
________________________________________________________________________。
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为_________________________________________。
(4)欲实现步骤Ⅴ,需加入的试剂有________、________,所涉及的主要操作依次为_____________。
(5)步骤Ⅳ常用的方法是________,该步骤是否对环境有影响?________(填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应:__________。
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl |
分别取四种物质进行实验,实验结果如下①B溶液分别与C、D混合,均有白色沉淀生成②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失③A与D两种固体混合有气体生成,该气体能使湿润的红色石蕊试液变蓝④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体
回答下列问题:
(1)A所含的阳离子和C所含阳离子的半径大小_▲___>___▲___(填离子符号)。B所含的阴离子是____▲____
(2)C溶液呈__▲_性(填“酸性”或“碱性”),其原因是______▲____________
(用离子方程式解释)。D的化学式是_____▲_______
(3)以Pt为电极电解1L0.1mol/LB的水溶液,当电路中通过0.1mol电子时,
溶液的pH为___▲____(设电解过程溶液体积不变),阳极的电极反应式为 ___▲__
(4)若将④阳极产生的气体通入A溶液中至恰好完全反应时,则溶液中各离子
浓度由大到小的排列顺序为____________▲______________
查看答案和解析>>
科目: 来源: 题型:
某溶液中可能含有Na+、NH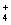 、Ba2+、SO
、Ba2+、SO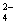 、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是
A. Na+ B.SO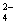 C. Ba2+ D.NH
C. Ba2+ D.NH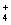
查看答案和解析>>
科目: 来源: 题型:
甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO 、SO
、SO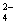 中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是
中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是
A.甲溶液含有Ba2+ B.乙溶液含有SO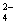
C.丙溶液含有Cl- D.丁溶液哈有Mg2+
查看答案和解析>>
科目: 来源: 题型:
某透明溶液中可能含有Fe2+、Fe3+、Al3+、NH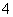 、Cl-、I-、NO
、Cl-、I-、NO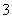 、SO
、SO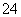 (H+、OH-没有列出)中的一种或几种,为了确认溶液中离子的存在情况,分别取等量的试液装入5支试管里,做如下实验:
(H+、OH-没有列出)中的一种或几种,为了确认溶液中离子的存在情况,分别取等量的试液装入5支试管里,做如下实验:
①测定溶液pH,pH=2;②向溶液中滴加过量氢氧化钠溶液,过滤、洗涤、灼烧、称重,得固体质量为3.2 g;③向溶液中加入过量浓氢氧化钠溶液,加热,收集到气体1.12 L(标准状况);④向溶液中加入足量的氯化钡溶液,过滤、洗涤、干燥、称重,得固体2.33 g;⑤向溶液中加入适量浓硫酸,再加入铜粉,振荡溶液,产生红棕色气体。下列对实验结论的分析合理的是 ( )
A.可能存在Al3+、Fe2+
B.只存在NO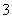 、NH
、NH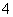 、SO
、SO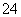 、Fe3+
、Fe3+
C.一定不存在Cl-、I-
D.可能存在Al3+、Cl-
查看答案和解析>>
科目: 来源: 题型:
在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2—、AlO2—、CO32-、SO32—、SO42—。某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3 溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2 溶液并加热,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同。
下列说法正确的是 ( )
A.气体甲可能为CO2 或者SO2
B.沉淀丙中一定含有BaCO3,可能含有BaSO4
C.该溶液中肯定存在的离子有K+、AlO2—、SO32—、SO42—、NO2—
D.只根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,K+是否存在无法确定
查看答案和解析>>
科目: 来源: 题型:
能正确表示下列反应的离子方程式为 ( )
A.碳酸氢钠溶液中滴入氢氧化钙溶液:HCO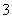 +OH-===CO
+OH-===CO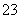 +H2O
+H2O
B.二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-===SO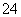 +Cl-+H2O
+Cl-+H2O
C.硫化钡加入稀硫酸:BaS+2H+===H2S↑+Ba2+
D.在强碱溶液中次氯酸钠与F e(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3===2FeO
e(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3===2FeO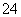 +3Cl-+H2O+4H+
+3Cl-+H2O+4H+
查看答案和解析>>
科目: 来源: 题型:
下表中评价合理的是 ( )
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀硝酸反应:2Fe3O4+18H+===6Fe3++H2↑+8H2O | 正确 |
| B | 向碳酸镁中加入稀盐酸:CO | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2===2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1∶2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com