
科目: 来源: 题型:
某化学反应过程如图所示。由图得出的判断, 正确的是 ( )
正确的是 ( )
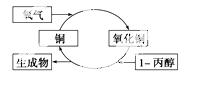
A.生成物是丙醛和丙酮
B.1丙醇发生了还原反应
C.反应中有红黑颜色交替变化的现象
D.醇类都能发生图示的催化氧化反应
查看答案和解析>>
科目: 来源: 题型:
年来,许多专家对石灰氮重新进行了深入研究,这也使得石灰氮这一古老的肥料又焕发了新的活力。石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、氮的质量分数分别为50 %、35%。石灰氮完全水解后的产物是固体A和气体B,其中B是制取氮肥的主要原料。固体A在高温下分解生成D和气体C。B的催化氧化产物为E和F,F继续氧化后的产物G遇到E生成一种工业强酸。将G和F的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液,该反应可表示如下G+F+H2O=2HNO2(已配平)。请回答下列问题:
%、35%。石灰氮完全水解后的产物是固体A和气体B,其中B是制取氮肥的主要原料。固体A在高温下分解生成D和气体C。B的催化氧化产物为E和F,F继续氧化后的产物G遇到E生成一种工业强酸。将G和F的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液,该反应可表示如下G+F+H2O=2HNO2(已配平)。请回答下列问题:
(1)石灰氮的化学式为 。
(2)足量B和C与饱和氯 化钠溶液的反应是化工生产中生产某种重要化工产品的重要反应,试写出其化学方程式
化钠溶液的反应是化工生产中生产某种重要化工产品的重要反应,试写出其化学方程式  。
。
(3)亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I— 被氧化为I2时,含氮产物为 (填化学式)。要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质中不适合使用是 (填序号)。
a、磷酸 b、二氧化碳 c、稀硫酸 d、二氧化硫 e、次氯酸
(4)工业废水中的NO2— 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。写出上述反应的离子方程式: 。
查看答案和解析>>
科目: 来源: 题型:
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

(2)整个过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为_ _色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若庄KI与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
查看答案和解析>>
科目: 来源: 题型:
氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO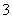 +4H++3e-===NO↑+2H2O.KMnO4、Na2C
+4H++3e-===NO↑+2H2O.KMnO4、Na2C O3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生
O3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生
(1)写出该氧化还原反应的化学方程式:________________________________________________。
(2)反应中硝酸体现了________、________.
(3)反应中若产生标准状况下11.2 L气体,则转移电子的物质的量是________mol.
(4)现称取含有杂质的甲样品(杂质与酸不反应)5.4 g,恰好与100 mL 1.4 mol/L的硝酸溶液完全反应,则该样品的纯度为________。
(5)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是_ _____________________
查看答案和解析>>
科目: 来源: 题型:
某同学探究SO2有关性质。
(1)将SO2通入BaCl2溶液中,将所得溶液分成2份,在第一份中加入NaOH溶液,在第二份中滴入FeCl3溶液,两份都有白色沉淀。BaCl2溶液中通入SO2气体的现象为 ▲ 。在第二份溶液中滴入FeCl3溶液时,SO2表现 ▲ 性,反应的离子方程式为 ▲ ,生成沉淀的化学式为 ▲ 。
(2)下列不能用来吸收SO2气体的是 ▲ 。
A.KMnO4(aq) B.过量氨水 C.石灰水 D.盐酸
查看答案和解析>>
科目: 来源: 题型:
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮氧化物(含NO、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2 +H2O。则生成的盐溶液中NaNO3的物质的量为
+H2O。则生成的盐溶液中NaNO3的物质的量为
A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 0.8 mol
查看答案和解析>>
科目: 来源: 题型:
有Fe2+、NO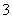 、Fe3+、NH
、Fe3+、NH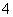 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是 ( )
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是 ( )
A.氧化剂与还原剂的物质的量之比为1∶8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.若有1 mol NO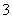 发生氧化反应,则转移8 mol e-
发生氧化反应,则转移8 mol e-
D.若把该反应设计为原电池,则负极反 应为Fe2+-e-===Fe3+
应为Fe2+-e-===Fe3+
查看答案和解析>>
科目: 来源: 题型:
①16H++10Z-+2XO4-→2X2++5Z2+8H2O ②2A2+ +B2→2A3++2B- ③2B-+Z2 →B2+2
→B2+2 Z-
Z-
由此判断下列说法错误的是
A.反应Z2+2A2+=2A3++2Z-可以进行。
B.Z元素在①③反应中均被还原
C.氧化性由强到弱的顺序是XO4-、Z2、B2、A 3+
3+
D.还原性由强到弱的顺序是A2+、B-、Z-、X2+
查看答案和解析>>
科目: 来源: 题型:
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl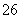 +6M,关于该反应
+6M,关于该反应 的说法中正确的组合是 ( )
的说法中正确的组合是 ( )
①氧化剂是H3AsO3 ②还原性:Cl->As ③每生成7.5 g As,还原剂失去的电子为0.3 mol
④M为OH- ⑤SnCl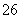 是氧化产物
是氧化产物
A.①③⑤ B.①②④⑤
C.①②③④ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com