
科目: 来源: 题型:
下列离子方程式正确的是
A.铝溶于稀硫酸:Al+2H+=Al3++H2↑,
B.铁粉溶于稀硫酸:Fe+2H+=Fe2++H2↑,
C.大理石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O,
D.氢氧化钡溶液和稀硫酸混合:Ba2++SO 42-=BaSO4↓。
查看答案和解析>>
科目: 来源: 题型:
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种。将纳米碳均匀分散到蒸馏水中得到一种分散系,下列有关该分散系的说法错误的是
A.属于溶液, B.能产生丁达尔效应,
C.分散质粒子能透过滤纸, D.静置不会析出黑色沉淀。
查看答案和解析>>
科目: 来源: 题型:
下列各组物质,其中有三组同时属于碱或同时属于酸性氧化物或同时属于混合物,另一组则不符合上述特点,该组物质是
A.烧碱和熟石灰,B.烧碱和纯碱,C.碘水和碘酒,D.二氧化碳和二氧化硫。
查看答案和解析>>
科目: 来源: 题型:
实验室用下图所示的装置制取乙酸乙酯。
 (1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,其操作步骤为 ____
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,其操作步骤为 ____ _______ ____________________________________,然后轻轻振荡试管使之混合均匀。
_______ ____________________________________,然后轻轻振荡试管使之混合均匀。
(2)装置中通蒸气的导管要插在饱和的Na2CO3溶液的液面上而不能插入溶液中,目的是防止溶液的倒吸。造成倒吸的原因是_______________________。
(3)浓硫酸的作用是:①__________________;②____________________。
(4)图中右边试管中试剂是_______________。
(5)分离得到乙酸乙酯的方法是__________,分离需要的玻璃仪器是____________________。
(6)若加的是C2H518OH写出制乙酸乙酯的方程式____________________________________。
(7)写出乙酸与碳酸氢钠反应方程式_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一。
(1)下列有关叙述正确的是__________(填写序号)
a.使用托盘天平的第一步操作是将游码移至标尺零刻度处
b.过滤操作过程中,为加快过滤速度可用玻璃棒对漏斗中的溶液进行搅拌
c.用浓硫酸配制稀溶液时,在量筒中衡稀后要冷却至室温再转移到容量瓶中
d.用容量瓶配制溶液时,定容后摇匀液面下降,再加蒸馏水至刻度线处,所得溶液浓度偏低
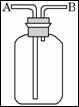 (2)现有六种气体:H2、O2、NH3、SO2、NO2、NO。可以利用如图所示装置进行收集。
(2)现有六种气体:H2、O2、NH3、SO2、NO2、NO。可以利用如图所示装置进行收集。
①若气体从B口进入,可收集的气体是_______________;
②若在烧瓶中注满水,则气体应该从___(填写“A”或“B”)口进入,可以收集的气体是_____。
查看答案和解析>>
科目: 来源: 题型:
铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)现配制100mL 0.01mol∙L-1 FeCl3溶液,配制过程中需要的玻璃仪器除量筒、胶头滴管、烧杯外,还需要 ,配制过程中除需用FeCl3固体、蒸馏水外,还需要的试剂有 。将已配制好的溶液滴入沸水中并煮沸一段时间,可得到红褐色液体,该反应的离子方程式为 ,此液体具有的性质是 (填字母)。
a.光束通过该液体时形成 光亮的“通路”
光亮的“通路”
b.向该液体中加入AgNO3溶液,无沉淀产生
c. 将该液体进行过滤,可得到红褐色固体
将该液体进行过滤,可得到红褐色固体
d.将该液体加热、 蒸干、灼烧后,有氧化物生成
蒸干、灼烧后,有氧化物生成
(2)在隔绝空气的条件下,用镁条引燃Fe3O4粉末和铝粉的均匀混合物,使其充分反应。
①向充分反应后的剩余固体中加入足量的NaOH溶液,有大量气泡产生,所得剩余固体中除铁外还含有的固体物质是 (填化学式)。
②已知:3Fe(s)+2O2(g)=Fe3O4(s) △H=−1118 kJ·mol-1
2Al(s)+3/2O2(g)=Al2O3(s) △H=−1675.7 kJ·mol-1
则铝与Fe3O4发生反应生成铁和 Al2O3的热化学方程式为 。
Al2O3的热化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
实验室用NaOH固体配制0.1 000mol·L-1NaOH溶液500mL.
 (1)用托盘天平称取NaOH固体________g.溶液配制过程用到下列玻璃仪器,按首次使用的先后顺序依次是_
(1)用托盘天平称取NaOH固体________g.溶液配制过程用到下列玻璃仪器,按首次使用的先后顺序依次是_ _______ (填仪器选项符号)
_______ (填仪器选项符号)
A.玻璃棒 B.胶头滴管
C.烧杯 D.500mL容量瓶
(2)用所配制的0.1000mol·L-1NaOH溶液通过中和滴定测定一元弱酸HA溶液浓度,每次滴定取用的HA溶液均为20.00mL,使用酚酞溶液为指示剂,滴定终点的标志是____________________________。滴定的实验数据记录:
| 滴定次数 | NaOH溶液体积(mL) | |
| V1 | V2 | |
| 1 | 3.05 | 44 |
| 2 | 1.45 | 41.5 |
| 3 | 7.65 | 47.6 |
处理以上实验数据,测得该HA溶液物质的量浓度为____________________。
(3)上述中和滴定实验中,以下操作可能导致所测溶液浓度偏高的是__________(填选项符号)
A.滴定管用待装液润洗 B.锥形瓶用待装液润洗
C.滴定前滴定管末端气泡没赶尽 D.滴定前平视观察读数,滴定后俯视观察读数
E.所用的标准液(NaOH溶液)浓度偏高
(4)用pH计测得该HA溶液pH=a,结合上述中和滴定结果可推算实验温度下HA的Ka=________。
查看答案和解析>>
科目: 来源: 题型:
下述实验方案能达到实验目的的是
| 编号 | A | B | C | D |
| 实验 方案 |
食盐水 |
|
|
置于光亮处 |
| 实验 目的 | 验证铁钉发生析氢腐蚀[ | 从碘与NaCl混合溶液中分离出碘 | 实验室制备乙炔 | 验证甲烷与氯气发生化学反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com