
科目: 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.黄绿色的氯水光照后颜色变浅
B.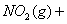
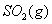
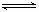
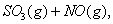 对该平衡体系加压后颜色加深
对该平衡体系加压后颜色加深
C.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目: 来源: 题型:
1体积气态烃和2体积氯化氢恰好完全发生反应后,其产物最多还能和8体积氯气发生取代反应,由此可以推断原气态烃是(气体体积均在相同条件下测定)( )
A.乙炔 B.1,3-丁二烯 C.戊炔 D.丙炔
查看答案和解析>>
科目: 来源: 题型:
下列与有机物结构、性质相关的叙述错误的是( )
A.用水可区分苯和溴苯
B.蛋白质和油 脂都属于高分子化合物,一定条件下都能水解
脂都属于高分子化合物,一定条件下都能水解
C.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同
D.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
化学与人类生活、社会可持续发展密切相关。下列措施有利于节能减排、保护环境的是( )
①加快化石燃料的开采与使用 ②研发易降解的生物农药 ③应用高效洁净的能源转化技术 ④田间焚烧秸秆 ⑤推广使用节能环保材料
A.①③⑤ B.②③⑤ C.①②④ D.②④⑤
查看答案和解析>>
科目: 来源: 题型:
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2 2O3。
2O3。
(1)若在上述反应中有30%的氧气转化为臭氧,计算所得混合气体的平均摩尔质量(保留一位小数)。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为多少L?
查看答案和解析>>
科目: 来源: 题型:
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
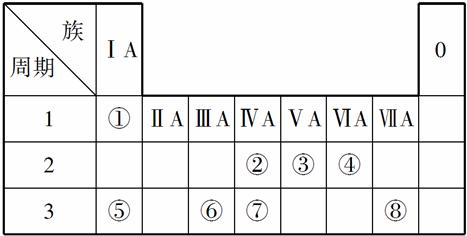
(1)④、⑤、⑥的原子半径由大到小的顺序为______________________。
(2)②、③、⑦三种元素的非金属性由强到弱的顺序是____________________。
(3)①、④、⑤、⑧中的三种元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:__________________。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
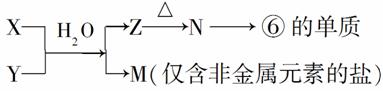
X溶液与Y溶液反应的离子方程式为______________________________,N→⑥的单质的化学方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,Y的单质在W2中燃烧的产物可使品红溶液褪色。Z的单质在W2中燃烧的产物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为________;XW的电子式为________;U元素在周期表中的位置是________________。
(2)U元素形成的同素异形体的晶体类型可能是(填序号,下同)________,Z单质的晶体类型是________。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、W的氢化物沸点较低的是(写化学式)________,比较V、W的氢化物的稳定性(写化学式)________________。
(4)YW2气体通入过量的NaOH溶液反应的离子方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上的电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(1)X的原子结构示意图为________。
(2)元素Y与氢元素形成一种离子YH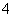 ,写出该微粒的电子式________(用元素符号表示)。
,写出该微粒的电子式________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
b. Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是(写出该种元素的最高价氧化物的水化物的化学式)________,理由是__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F为原子序数依次增大的同周期的主族元素,已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4,E元素原子次外层电子数比最外层电子数多3。请回答下列问题:
(1)写出下列元素的符号:B________、D________、E________。
(2)写出B、F形成的化合物的电子式________________________________________________________________________。
(3)A、C两种元素最高价氧化物的水化物反应的离子方程式:________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com