
科目: 来源: 题型:
下列叙述中正确的是( )
A.在多电子的原子里,能量高的电子通常在离核近的区域内运动
B.核外电子总是先排在能量低的电子层上
C.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
D.微粒的最外层只能是8个电子才稳定
查看答案和解析>>
科目: 来源: 题型:
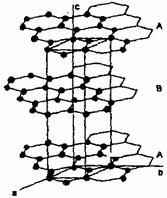 石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如右图所示,图中用虚线标出了石墨的一个六方晶胞。
石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如右图所示,图中用虚线标出了石墨的一个六方晶胞。
(1)该晶胞的碳原子个数 。
(2)写出晶胞内各碳的原子坐标。
(3)已知石墨的层间距为334.8 pm,C-C键长为142 pm,计算石墨晶体的密度为 。
 石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
(4)右图给出了一个Li+沿C轴投影在A层上的位置,试在右图上标出与该离子临近的其他6个Li+的投影位置。
(5)在LiC6中,Li+与相邻石墨六元环的作用力属何种键型?
(6)某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式。

查看答案和解析>>
科目: 来源: 题型:
某同学在学习等径球最密堆积(立方最密堆积A1和六方最密堆积A3)后,提出了另一种最密堆积形式Ax 。如右图所示为Ax 堆积的片层形式,然后第二层就堆积在第一层的空隙上。请根据Ax 的堆积形式回答:
(1)计算在片层结构中(如右图所示)球数、空隙数和切点数之比
(2)在Ax 堆积中将会形成正八面体空隙和正四面体空隙。请在片层图中画出正八面体空隙(用·表示)和正四面体空隙(用×表示)的投影,并确定球数、正八面体空隙数和正四面体空隙数之比
(3)指出Ax 堆积中小球的配位数
(4)计算Ax 堆积的原子空间利用率。
(5)计算正八面体和正四面体空隙半径(可填充小球的最大半径,设等径小球的半径为r)。
(6)已知金属Ni晶体结构为Ax 堆积形式,Ni原子半径为124.6 pm,计算金属Ni的密度。(Ni的相对原子质量为58.70)
(7)如果CuH 晶体中Cu+的堆积形式为Ax 型,H- 填充在空隙中,且配位数是4。则H- 填充的是哪一类空隙,占有率是多少?
(8)当该同学将这种Ax 堆积形式告诉老师时,老师说Ax 就是A1或A3的某一种。你认为是哪一种,为什么?
查看答案和解析>>
科目: 来源: 题型:
最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行(面心)立方最密堆积(ccp),它们的排列有序,没有相互代换的现象(即没有平均原子或统计原子),它们构成两种八面体空隙,一种由镍原子构成,另一种由镍原子和镁原子一起构成,两种八面体的数量比是1︰3,碳原子只填充在镍原子构成的八面体空隙中。
(1)画出该新型超导材料的一个晶胞(碳原子用小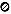 球,镍原子用大○球,镁原子用大
球,镍原子用大○球,镁原子用大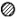 球)。
球)。
(2)写出该新型超导材料的化学式。
查看答案和解析>>
科目: 来源: 题型:
已知Fe x O晶体的晶胞结构为NaCl型,由于晶体缺陷,x的值小于1。测知Fe x O晶体密度ρ为5.71g·cm–3,晶胞边长为4.28×10–10m(铁原子量为55.9,氧原子量为16.0)。求:
(1)FexO中x的值(精确至0.01)。
(2)晶体中的Fe分别为Fe2+ 和Fe3+,在Fe2+ 和Fe3+ 的总数中,Fe2+所占分数为多少?(精确至0.001。)
(3)写出此晶体的化学式。
(4)描述Fe在此晶体中占据空隙的几何形状(即与O2– 距离最近且等距离的铁离子围成的空间形状)。
(5)在晶体中,铁元素的离子间最短距离为多少?
查看答案和解析>>
科目: 来源: 题型:
C70分子是形如椭球状的多面体,该结构的建立基于以下考虑:
(1)C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;
(2)C70分子中只含有五边形和六边形;
(3)多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数 + 面数-棱边数= 2。
根据以上所述确定:
(1)C70分子中所含的单键数和双键数;
(2)C70分子中的五边形和六边形各有多少个?
查看答案和解析>>
科目: 来源: 题型:
晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子,如图所示。
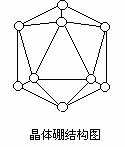
回答:
(1)键角 ____________ ;(2)晶体硼中的硼原子数______________个;
(3)B–B键_____________条?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com