
科目: 来源: 题型:
已知:
① 在稀碱溶液中,溴苯难发生水解
②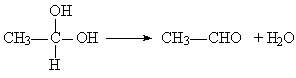
现有分子式为C10H10O2Br2的芳香族化合物X,其苯环上的一溴代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。
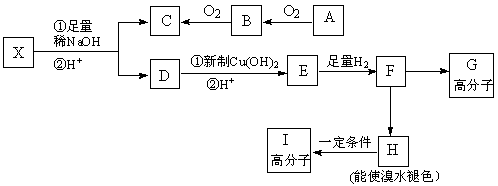

请回答下列问题:
(1)X中官能的名称是 。
(2)F→H的反应类型是 。
(3)I的结构简式为 。
(4)E不具有的化学性质 (选填序号)。
a.取代反应 b.消去反应 c.氧化反应 d.1molE最多能与2molNaHCO3反应
(5)写出下列反应的化学方程式:
① X与足量稀NaOH溶液共热的化学方程式: 。
② F→G的化学方程式: 。
(6)同时符合下列条件的E的同分异构体共有 种,其中一种的结构简式为 。
a.苯环上核磁共振氢谱有两种 b.不能发生水解反应
c.遇FeCl3溶液不显色 d.1molE最多能分别与1molNaOH和2molNa反应
查看答案和解析>>
科目: 来源: 题型:
尿素[CO(NH2)2]是一种非常重要的高氮化肥,以天然气(含H2S)为原料合成尿素的主要步骤如下图所示(图中某些转化步骤未列出)。

请回答下列问题:
(1)反应①的离子方程式是__________ ____
(2)天然气脱硫后产生的Fe2S3和H2O与02反应的化学方程式是__ _____。
(3)反应②N2+3H2 2NH3 △H<0,温度升高,该反应的平衡常数_______ (填 “增大”、“减小” 或“不 变”)。如 该反应在恒容恒温条件下进行,下列说法能判断达到平衡的是 。
2NH3 △H<0,温度升高,该反应的平衡常数_______ (填 “增大”、“减小” 或“不 变”)。如 该反应在恒容恒温条件下进行,下列说法能判断达到平衡的是 。
A.单位时间内生成nmol N2同时消耗3nmol H2 B.混合气体的密度不变
C.混合气体的平均摩尔质量不变 D. N2、H2、NH3浓度之比为1:3:2
(4)H2NCOONH4 (氨基甲酸铵)是合成尿素的中间体,H2NCOONH4在水溶液中要发生水解反应,其水解反应的离子方程式为:____ __。
 (5)如果整个生产过程釆用绿色化学工艺,则生产120t尿素理论上需要CH4__ _m3 (标准状况)。
(5)如果整个生产过程釆用绿色化学工艺,则生产120t尿素理论上需要CH4__ _m3 (标准状况)。
(6) 化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电。尿素燃料电池结构如图所示,工作时负极的电极反应式为______ ____。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组研究HNO3的氧化性,设计了如下实验:
在盛有新制FeSO4溶液的试管中滴入2滴KSCN溶液,观察现象,然后再滴入几滴浓HNO3,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色快速变为蓝色,并产生红棕色气体,这一奇特现象激起了同学的好奇心与求知欲望,对此现象设计了探究性实验。
⑴甲同学认为是溶液中的Fe2+的干扰造成的,大家经过理性分析,认为可以排除Fe2+的干扰,理由是______________________________________________。
⑵乙同学认为红色消失,说明Fe(SCN)3被破坏,红棕色NO2说明了某些离子与HNO3发生了氧化还原,推测可能是KSCN与HNO3作用。KSCN溶液是一种无色液体,根据C、S、N的原子结构和共价键的相关知识推测SCN-中碳原子的杂化轨道类型是_______杂化。
⑶根据乙同学的观点,设计了实验方案1,往浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色,突然剧烈反应产生大量气泡,放出红棕色气体,而溶液红色消失变为浅绿色,溶液温度升高;继续滴入KSCN,溶液变为浅蓝色,最后变成无色。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种非极性气体;向反应后的溶液中加入BaCl2溶液产生白色沉淀,写出向浓HNO3中滴入KSCN的离子方程式__________________________________________________________________。
⑷丙同学认为SCN-的性质还可进一步探究,设计了方案2,向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均消失变为黄色,而加入碘水时溶液的颜色基本不变。丙同学的设计意图是__________________________________________________。
⑸通过本次探究,可以得出以下结论:
a、用SCN-间接检验Fe2+时应注意__________;b、与SCN-反应使溶液变红的______是Fe3+。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是____,F元素的原子基态价层电子排布式__ 。
(2) 分子的电子式为__________,
分子的电子式为__________, 分子的空间立体构型为__________。
分子的空间立体构型为__________。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________、I:__________。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________。
 (5)0.3g H在足量氧气中燃烧,生成气态
(5)0.3g H在足量氧气中燃烧,生成气态 和液态
和液态 ,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。
,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________。
查看答案和解析>>
科目: 来源: 题型:
已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中,不正确的是
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中,不正确的是
A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为6 mol
C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
查看答案和解析>>
科目: 来源: 题型:
下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
C.pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中:c(NH )大小顺序:①>②>③
)大小顺序:①>②>③
D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
查看答案和解析>>
科目: 来源: 题型:
在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol/(L·min
mol/(L·min )
)
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是( )。
A.向漂白粉溶液中通入少量SO2气体:Ca2++ClO-+SO2+H2O===CaSO4↓+2H++Cl-
B.向盐酸中逐滴加入等体积等浓度的碳酸钠溶液:CO32-+2H+==CO2↑+H2O
C.KHC2O4使酸性KMnO4溶液褪色:5C2O42-+16H++2MnO4-===10CO2↑+ 2Mn2++8H2O
D.向银氨溶液中加入足量的氢碘酸溶液:〔Ag(NH3)2〕++OH-+3H+= Ag++H2O +2NH4+
查看答案和解析>>
科目: 来源: 题型:
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3+2HI=2FeCl2+I2+2HCl;2Co(OH)3+ 6HCl =2CoCl2+Cl2↑+6H2O[来源 :2Fe(OH)2+ I2+2KOH = 2Fe(OH)3+2KI; 3I2+6KOH=5KI+KIO3+3H2O
6HCl =2CoCl2+Cl2↑+6H2O[来源 :2Fe(OH)2+ I2+2KOH = 2Fe(OH)3+2KI; 3I2+6KOH=5KI+KIO3+3H2O
复分解反应:2HSCN +K2CO3 = 2KSCN + CO2 ↑ + H2O; KCN + CO2 + H2O = HCN + KHCO3

 热分解反应:4NaClO 3NaCl + Na
热分解反应:4NaClO 3NaCl + Na ClO4;NaClO4 NaCl + 2O2↑
ClO4;NaClO4 NaCl + 2O2↑
下列说法不正确是 ( )
A.酸性(水溶液):HSCN > H2CO3 > HCN B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3
C.热稳定性:NaCl > NaClO4 > NaClO D.氧化性(酸性溶液):FeCl3 > Co(OH)3 > I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com