
科目: 来源: 题型:
有一种纸质软电池,该电池采用薄层纸片作为载
 体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为
体和传导体,一面附着锌,另一面附着二氧化锰。电池总反应为
Zn+2MnO2+H2O===ZnO+2MnO(OH),关于此电池,下列说法正确的是
A.该电池Zn为负极,ZnO为正极,MnO2催化剂]
B.该电池的正极反应为MnO2+e-+H2O===MnO(OH)+OH-
C.放电时外电路电子由Zn流向MnO2,内电路电子由M nO2流向Zn
nO2流向Zn
D.电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动
查看答案和解析>>
科目: 来源: 题型:
为充分利用海洋资源,研究人员发明海水电池,这
种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表 示为:
示为:
5MnO2+2Ag+2NaCl=Na2 Mn5O10+2AgCl
Mn5O10+2AgCl
下列说法错误的是
A.负极反应式: Ag+Cl——e-=AgCl B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Cl—不断向电池的正极移动 D.Na2Mn5O10是还原产物
查看答案和解析>>
科目: 来源: 题型:
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,
该电池主要工作原理如右图所示,其正极反应为:ClO- + H2O + 2e- == Cl- + 2OH-,关于该电池的叙述正
确的是
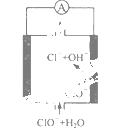 A.该电池中镁为负极,发生还原反应
A.该电池中镁为负极,发生还原反应
B.电池工作时,OH-向正极移动
C.电池工作时,正极周围溶液的pH将不断变小
D.该电池的总反应为:Mg + C lO- + H2O == Mg(OH)2↓+ Cl-
lO- + H2O == Mg(OH)2↓+ Cl-
查看答案和解析>>
科目: 来源: 题型:
将两金属A、B分别用导线相连接,并同时插入电解质溶液中,发现A极的质量增加,则下列说法正确
的是 ( )
A.金属活动性:A>B
B.A极是正极,电解质溶液可以是盐酸
C.B极是负极
D.要判 断A极与B极是正极还是负极,还需考虑电解质溶液
断A极与B极是正极还是负极,还需考虑电解质溶液
查看答案和解析>>
科目: 来源: 题型:
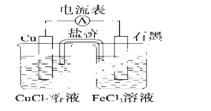
控制合适的条件,将反应2Fe3++2I-  2Fe2+I2设计成如下图所示
2Fe2+I2设计成如下图所示
的原电池。下列说法不正确的是
A.盐桥中的K+移向FeCl3溶液
B.反应开始时,乙中石墨电极上发生氧化反应
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
查看答案和解析>>
科目: 来源: 题型:
关于原电池的叙述正确的是 ( )
A.原电池工作时,电极上不一定都发生氧化还原反应
B.某可逆电流充、放电时的反应式为Li1-xNiO2+xLi LiNiO2,放电时此电池的负极材料是Li1-xNiO2
LiNiO2,放电时此电池的负极材料是Li1-xNiO2
C.铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1 120 mL(标准状况)气体析出
D.在理论上可将反应CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH<0设计成原电池
查看答案和解析>>
科目: 来源: 题型:
上海世博会期间,在德国馆的汉堡之家展馆人们看到一个1∶20飞机燃料电池的模型。燃料电池是一
种通过氢氧结合来发电的电化学装置。某氢氧燃料电池的电池反应为2H2+O2===2H2O,电解液为KOH溶
液。氢氧燃料电池的突出优点是把________能直接转化为________能,而不用经过________能这一中间形
式。
 (1)有关氢氧燃料电池的下列叙述中,正确的是 ( )
(1)有关氢氧燃料电池的下列叙述中,正确的是 ( )
A.此电池能发出蓝色火焰
B.氢气为正极,氧气为负极
C.因为生成水,所以工作时溶液的碱性越来越强
D.负极上氢气失电子,发生氧化反应;正极上氧气得电子,发生还原反应
(2)该电池所产生的水可以作为饮用水,今欲制得 常温下1 L水,则电池内转移电子的物质的量为________。
常温下1 L水,则电池内转移电子的物质的量为________。
A.8.9×10-3 mol B.4.5×10-2 mol
C.1.1×102 mol D.5.6×103 mol
查看答案和解析>>
科目: 来源: 题型:
铝空气海水电池:以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。
电池总反应为4Al+3O2+6H2O===4Al(OH)3
负极:______________________________________________________________;
正极:______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
控制适合的条件,将反应2Fe3++2I-=2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是( )
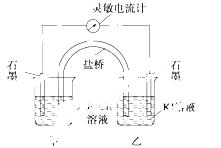 A.反应开始时,乙中石墨电极上发生氧化反应
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目: 来源: 题型:
某小组为研究原电池原理,设计如图装置,下列叙述正确的是
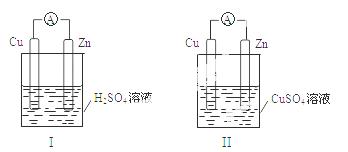
A.装置I,铜片上有O 2逸出
2逸出
B.装置I,锌片溶解,发生还原反应
C.装置II,电池反应为:Zn+ Cu2+= Zn2++ Cu
D.装置II,外电路中,电子从锌电极流向铜电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com