
科目: 来源: 题型:
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
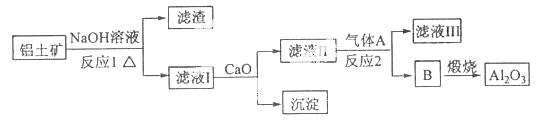
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
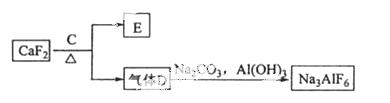
回答下列问题:
(1)写出反应1的化学方程式 , ;
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2的离子方程式为 ;
(3)E可作为建筑材料,化合物C是 ,写出由D制备冰晶石的化学方程式 ;
(4)电解制铝的化学方程式是 ,以石墨为电极,阳极产生的混合气体的成分是 。
查看答案和解析>>
科目: 来源: 题型:
“科学与技术”模块(10分)
电石浆是氯碱工业中的一种废弃物,其大致组成如 下表所示:
下表所示:
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其它不溶于酸的物质 |
| 质量分数(%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水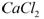 ,某化工厂设计了以下工艺流程:
,某化工厂设计了以下工艺流程:
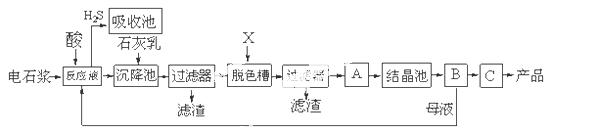
已知氯化钙晶体的化学式是:CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中 加入的酸应选用 。
加入的酸应选用 。
(2)脱色槽中应加入的物质X是 ‚ ;设备A的作用是 ƒ ;设备B的名称为 ④ ;设备C的作用是 ⑤ 。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是 ⑥ 。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是 ⑦ 。
查看答案和解析>>
科目: 来源: 题型:
下列解释事实的方程式不准确的是
A.用浓盐酸检验氨:NH3 +HC1=NH4C1
+HC1=NH4C1
B.碳酸钠溶液显碱性:CO2-3+H2O HCO-3+OH-
HCO-3+OH-
C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
下列物质性质与应用对应关系正确的是
A.晶体硅熔点高硬度大,可用于制作半导体材料
B.氢氧化铝具有弱碱性,可用于制胃酸中和剂
C.漂白粉在空气中不稳定,可用于漂白纸张
D.氧化铁能与酸反应,可用于制作红色涂料
查看答案和解析>>
科目: 来源: 题型:
(1)(2010·江苏,8D)相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 ( )
(2)(2010·广东理综,22D)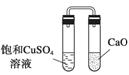 实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 ( )
实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 ( )
(3)(2009·广东,5②)四川灾区重建使用了大量钢材,钢材是合金 ( )
(4)(2009·山东理综,9A)合金材料中可能含有非金属元素 ( )
(5)(2008·山东理综,9A)金属材料都是导体,非金属材料都是绝缘体 ( )
查看答案和解析>>
科目: 来源: 题型:
实验室中用含少量CO2杂质的CO来还原铁的氧化物Fe xOy,并证明CO能够还原FexOy,且本身被氧
xOy,并证明CO能够还原FexOy,且本身被氧
化为CO2,实验所提供的各种仪器和药品如下:
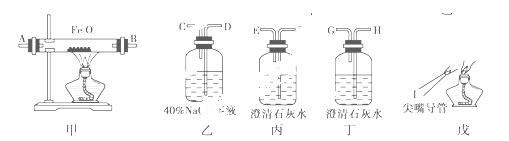
(1)实验时,上述仪器装置的正确连接顺序是(填写各接口的代号)。混合气体—→________,________接(F),(E)接________,________接________,________接________。
(2)在装置乙中发生反应的化学方程式是
__________________________________________________________________。
(3)在装置甲中发生反应的化学方程式是______________________________。
(4)丙装置中澄清石灰水的作用是__________________________________________。
(5)经定量测定,0.4 g FexOy与CO反应生成的气体通入过量的澄清石灰水中,生成0.75 g白色沉淀,则FexOy中x值是________,y值是________。
(6)实验过程中,能说明CO能够还原FexOy的实验现象是________;能够说明CO被氧化成CO2的实验现象是_______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
海水是镁的主要来源之一 。从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水
。从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水
中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物。
(1)以上提取镁的全过 程中,没有涉及的化学反应类型是________(填序号)。
程中,没有涉及的化学反应类型是________(填序号)。
A.分解反应 B.化合反应
C.置换反应 D.复分解反应
(2)下列关于提取镁的说法中,不正确的是______(填序号)。
A.此法的优点之一是原料来自大海
B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁
D.电解冶炼镁要消耗大量电能
查看答案和解析>>
科目: 来源: 题型:
有0.4 g铁的氧化物用足量的CO在高温下将其还原,把生成的全部CO2通入足量澄清石灰水中,得到
0.75 g固体沉淀物。这种铁的氧化物的化学式为( )
A.FeO B.Fe2O3 C.Fe3O4 D.FeO、Fe2O3
查看答案和解析>>
科目: 来源: 题型:
已知MgO、MgCl2的熔点分别为2 800 ℃、604 ℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁正确的方法是( )
A.海水 Mg(OH)2
Mg(OH)2 Mg
Mg
B.海水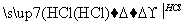 MgCl2溶液—→MgCl2(熔融)
MgCl2溶液—→MgCl2(熔融) Mg
Mg
C.海水 Mg(OH)2
Mg(OH)2 MgO
MgO Mg
Mg
D.海水 Mg(OH)2
Mg(OH)2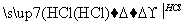 MgCl2溶液—→M
MgCl2溶液—→M gCl2(熔融)
gCl2(熔融) Mg
Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com