
科目: 来源: 题型:
下表所列数据是某高温下金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验记录,a和b均为与温度有关的常数。
| 反应时间t/h | 1 | 4 | 9 | 16 | 25 |
| MgO层厚y/nm | 0.05a | 0.20a | 0.45a | 0.80a | 1.25a |
| NiO层厚y′/nm | b | 2b | 3b | 4b | 5b |
(1)金属在高温下的氧化腐蚀速率可以用金属氧化膜的生成速率来表示,其理由是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)金属氧化膜的膜厚y跟时间t所呈现的关系是:MgO氧化膜的膜厚y属于________型,NiO氧化膜的膜厚y′则属于________型。(填“直线”或“抛物线”或“双曲线”或“对数”等类型)
(3)Mg与Ni相比较,金属________具有更好的耐氧化腐蚀性,其理由是
________________________________________________________________________
______________________________。
查看答案和解析>>
科目: 来源: 题型:
在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.6 g 纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min 末收集到氢气1.12 L(标况),在此之后,又经过4 min 铁粉全部溶解。则:
(1)在前2 min内用FeCl2表示的平均反应速率是多少?
(2)在后4 min内用HCl表示的平均反应速率是多少?
(3)前2 min与后4 min相比,反应速率哪个较快?为什么?试解释原因。
查看答案和解析>>
科目: 来源: 题型:
某温度时在2 L容器中X、Y、Z三种气态物质的变化曲线如图所示:
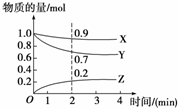
由图中数据分析该反应的化学方程式:
________________________________________________________________________。
反应开始至2 min末Z的平均反应速率为
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
反应A(g)+3B(g)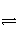
 2C(g)+2D(g)在四种不同情况下的反应速率,分别为
2C(g)+2D(g)在四种不同情况下的反应速率,分别为
①vA=0.015 mol·L-1·s-1 ②vB=0.06 mol·L-1·s-1 ③vC=0.04 mol·L-1·s-1
④vD=2.7 mol·L-1·min-1
该反应的快慢顺序为______________________(填序号)。
查看答案和解析>>
科目: 来源: 题型:
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时
间变化的曲线如右图。下列叙述中正确的是( )
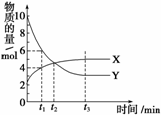
A.反应的化学方程式为5Y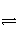
 X
X
B.t1时,Y的浓度是X浓度的1.5倍
C.t2时,正、逆反应速率相等
D.t3时,逆反应速率大于正反应速率
查看答案和解析>>
科目: 来源: 题型:
化合物Bilirubin在一定波长的光的照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
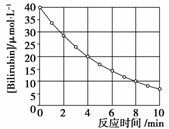
A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
科目: 来源: 题型:
一定温度下,向一个容积为2 L的真空密闭容器中(事先装入催化剂)通入1 mol N2和3 mol H2,发生下列反应:N2(g)+3H2(g)
 2NH3(g),3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
2NH3(g),3 min后测得密闭容器内的压强是起始时的0.9倍,在此时间内v(H2)是( )
A.0.2 mol·L-1·min-1 B.0.6 mol·L-1·min-1
C.0.1 mol·L-1·min-1 D.0.3 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
反应:2SO2(g)+O2(g)
 2SO3(g)经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为( )
2SO3(g)经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为( )
A.0.1 s B.2.5 s C.10 s D.5 s
查看答案和解析>>
科目: 来源: 题型:
把0.6 mol X气体和0.6 mol Y气体混合于2 L的容器中,使它们发生如下反应:3X(g)+Y(g)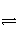
 nI(g)+2W(g),5 min 末生成0.2 mol W,若测得以I的浓度变化表示的平均反应速率为0.01 mol·L-1·min-1,则化学反应方程式中的n值为( )
nI(g)+2W(g),5 min 末生成0.2 mol W,若测得以I的浓度变化表示的平均反应速率为0.01 mol·L-1·min-1,则化学反应方程式中的n值为( )
A.4 B.3 C.2 D.1
查看答案和解析>>
科目: 来源: 题型:
反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)在10 L 密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率
4NO(g)+6H2O(g)在10 L 密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率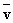 (X)可表示为( )
(X)可表示为( )
A.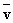 (NH3)=0.010 mol·L-1·s-1
(NH3)=0.010 mol·L-1·s-1
B.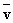 (O2)=0.001 0 mol·L-1·s-1
(O2)=0.001 0 mol·L-1·s-1
C.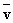 (NO)=0.001 0 mol·L-1·s-1
(NO)=0.001 0 mol·L-1·s-1
D.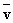 (H2O)=0.045 mol·L-1·s-1
(H2O)=0.045 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com