
科目: 来源: 题型:
某有机化合物的结构简式为: ,下列有关该物质的叙述正确的是
,下列有关该物质的叙述正确的是
A. 1 mol该物质最多可以消耗3 mol Na
B.1 mol该物质最多可以消耗7 mol NaOH
C.不能与Na2CO3溶液反应
D.易溶于水,可以发生加成反应和取代反应
查看答案和解析>>
科目: 来源: 题型:
已知: ,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。
,从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体。

回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个互为对位取代基的化合物有4种,其结构简式为_______________,_________________,_______________,______________。
(4)A的结构简式可能为_______________________________________(只写一种即可)。
查看答案和解析>>
科目: 来源: 题型:
阿司匹林的有效成分是乙酰水杨酸( )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:

操作流程如下:

已知:水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,醋酸酐遇水分解生成醋酸。
回答下列问题:
(1)合成过程中最合适的加热方法是 。
(2)制备过程中,水杨酸会形成聚合物的副产物。写出该聚合物的结构简式 。
(3)粗产品提纯:
① 分批用少量饱和NaHCO3溶解粗产品,目的是 。判断该过程结束的方法是 。
② 滤液缓慢加入浓盐酸中,看到的现象是 。
③ 检验最终产品中是否含有水杨酸的化学方法是 。
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):Ⅰ.称取阿司匹林样品m g;
Ⅱ.将样品研碎,溶于V1 mL a mol·L-1NaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;
Ⅲ.向锥形瓶中滴加几滴甲基橙,用浓度为b mol·L-1的标准盐酸到滴定剩余的NaOH,消耗盐酸的体积为V2mL。
① 写出乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式: 。
② 阿司匹林药片中乙酰水杨酸质量分数的表达式为 。
查看答案和解析>>
科目: 来源: 题型:
[化学—选修5:有机化学基础)(15分)
二苯乙烯类化合物苯烯莫德中文别名(E)-3,5-二羟基-4-异丙基二苯乙烯,是新一代消炎药物,可用于治疗多种重大自身免疫性疾病,如牛皮癣、湿疹、发浓性结肠炎和多种过敏性疾病。其合成路线如下:

已知:

(1)B中含氧官能团名称是___________________。
(2)B- C的反应类型是_____________反应,E的结构简式是___________________________。
(3)下列有关说法正确的是(填字母序号)。
a. B的核磁共振氢谱有4组峰
b.1mol D一定条件下加成最多消耗4 mol H2
c. F不存在顺反异构体
d.苯烯莫德一定条件下可以发生取代反应、加成反应、氧化反应、加聚反应等
(4)写出苯烯莫德与 发生缩聚反应生成高分子化合物H的化学方程式:___________________。
发生缩聚反应生成高分子化合物H的化学方程式:___________________。
(5)化合物A有多种同分异构体:
①能够发生银镜反应和水解反应,同时1 mol该物质与足最的NaOH溶液发生反应最多可以消耗4 mol NaOH的共有_____________种;
②能够发生银镜反应但不能发生水解反应,同时遇到三氯化铁溶液可显紫色并且相同的官能团连在相邻的碳原子上的共有种____________。
查看答案和解析>>
科目: 来源: 题型:
丙烯酸乙酯(化合物Ⅳ)是制备塑料、树脂等高聚物的重要中间体,可由下面路线合成:
 (1)化合物Ⅳ的分子式为 ,1 mol化合物Ⅳ完全燃烧消耗O2为 mol。
(1)化合物Ⅳ的分子式为 ,1 mol化合物Ⅳ完全燃烧消耗O2为 mol。
(2)化合物Ⅱ能使溴水褪色,其反应方程式为 。
(3)反应②属于 反应,化合物Ⅰ可以由化合物Ⅴ(分子式为C3H6O)催化氧化得到,则化合物Ⅴ→Ⅰ的反应方程式为 。
(4)化合物Ⅵ是化合物Ⅳ的同分异构体,Ⅵ含有碳碳双键并能与NaHCO3溶液反应放出气体,其核磁共振氢谱峰面积之比为1:1:6,则化合物Ⅵ的结构简式为 。
(5)一定条件下,化合物  也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 。
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:
有机物A~F有如下转化关系:
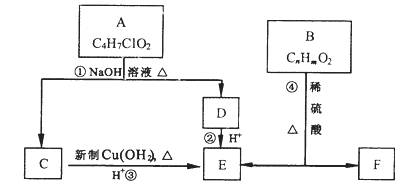
已知一个碳原子上连有两个羟基时不稳定,转化如下:

请回答:
(1)A的结构简式为: ;④的反应类型
(2)C与新制Cu(OH)2的化学方程式为
(3)已知B的摩尔质量为162g/mol,完全燃烧的产物中n(CO2):n(H2O)=2:1,B的分子式为 。
(4)F是生产高分子光阻剂的主要原料,特点如下:
①能发生加聚反应 ②含有苯环且苯环上一氯取代物只有两种 ③遇FeCl3显紫色
F与浓溴水反应的化学方程式
B与NaOH反应的化学方程式
(5)F的一种同分异构体G含苯环且能发生银镜反应。写出一种满足条件的G的结构简式
查看答案和解析>>
科目: 来源: 题型:
实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示)。
 (1)制备实验开始时,先检查装置气密性,接下来的操作依次是_______(填序号)。
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是_______(填序号)。
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,
探究小组同学提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
丁方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:
①判定甲方案不可行,理由是____________________________________________。
②进行乙方案实验:准确量取残余清液稀释一定倍数 后作为试样。
后作为试样。
 a.量取试样20.00 mL,用0.100 0 mol·L-1 NaOH标准溶液滴定,消耗22.00 mL,该次滴定测得试样中盐酸浓度为__________mol·
a.量取试样20.00 mL,用0.100 0 mol·L-1 NaOH标准溶液滴定,消耗22.00 mL,该次滴定测得试样中盐酸浓度为__________mol· L-1;
L-1;
b.平行滴定后获得实验结果。
③判断丙方案的实验结果________(填“偏大”、“偏小”或“准确”)。
[已知:Ksp(CaCO3)=2.8×10-9、Ksp(MnCO3)=2.3×10-11]
④进行丁方案实验:装置如右图所示(夹持器具已略去)。
(ⅰ) 使Y形管中的残余清液与锌粒反应的正确操作是将________ 转移到________中。
(ⅱ)反应完毕,每间隔1分钟读取气体体积,气体体积逐次减小,直至不变。气体体积逐次减小的原因是_____________
(排除仪器和实验操作的影响因素)。
查看答案和解析>>
科目: 来源: 题型:
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成。
(1)实验室中常用来制备氯气的化学方程式为____________________________。
(3)实验室中可用氯仿(CHCl3)与双氧水直接反应制备光气,
其反应的化学方程式为______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下图所示是验证氯气性质的 微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
查看答案和解析>>
科目: 来源: 题型:
下列与含氯化合物有关的说法正确的是 ( )
A.HClO是弱酸,所以NaClO是弱电解质
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com