
科目: 来源: 题型:
下列说法正确的是( )
A.pH<7的溶液不一定是酸溶液
B.常温下,pH=5的溶液和pH=3的溶液相比,前者[OH-]不一定是后者的100倍
C.室温下,每1×107个水分子中只有一个水分子发生电离
D.在1 mol·L-1的氨水中,改变外界条件使[NH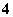 ]增大,则溶液的pH一定增大
]增大,则溶液的pH一定增大
查看答案和解析>>
科目: 来源: 题型:
下列溶液一定显酸性的是( )
A.溶液中[OH-]>[H+]
B.滴加紫色石蕊试液后变红色的溶液
C.溶液中[H+]=10-6 mol·L-1
D.pH<7的溶液
查看答案和解析>>
科目: 来源: 题型:
1.下列溶液一定呈中性的是( )
A.pH=7的溶液
B.[H+]=[OH-]的溶液
C.由强酸、强碱等物质的量反应得到的溶液
D.非电解质溶于水得到的溶液
查看答案和解析>>
科目: 来源: 题型:
将一定质量的铁粉加入到装有100 mL某浓度的稀硝酸溶液中充分反应。
(1)容器中剩有m g的铁粉,收集到NO气体448 mL(标准状况下)。
①所得溶液中的溶质的化学式为________________。
②原硝酸溶液的物质的量浓度为__________________________。
(2)向上述固液混合物中逐渐滴加稀硫酸直至刚好不再产生气体为止,该气体遇空气变成红棕色。此时容器中有铁粉n g。
①此时溶液中溶质的化学式为__________________。
②(m-n)的值为________________(精确到0.1 g)。
查看答案和解析>>
科目: 来源: 题型:
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2的漂白性。
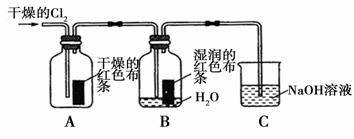
①通入Cl2后,观察到的现象是 根据现象可得出的结论是 。
②集气瓶B发生反应的离子方程式是 。
③C装置的作用是 ,若有2.24 L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为________mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
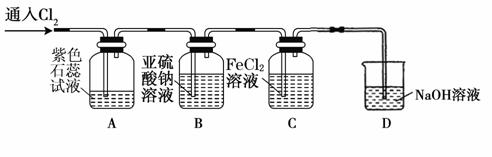
①实验开始后,观察装置A中的现象是 。
②装置C中发生反应的离子方程式是 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2时装置B中发生反应的离子方程式是 。
查看答案和解析>>
科目: 来源: 题型:
回答实验室配制0.1 mol/L的NaOH溶液480 mL实验中的下列问题。
(1)需NaOH_________g。
(2)有以下仪器:①烧杯 ②100 mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶
⑤玻璃棒 ⑥托盘天平。 配制时,必须使用的仪器有____________________,
还缺少的仪器是__________________。
(3)下列称量NaOH的操作中,正确的是_______________(填序号,下同)
①把NaOH直接放在托盘上称量 ②把NaOH放在纸上称量
③把NaOH放入烧杯中称量
(4)使用容量瓶前必须进行的一步操作是_______________________________。
(5)配制过程中,下列操作会引起浓度偏高的是_______________________。
①未洗涤烧杯、玻璃棒 ②NaOH溶液未冷却至室温就转移到容量瓶中
③容量瓶不干燥,含有少量蒸馏水 ④称量NaOH的时间太长
⑤定容时俯视刻度
查看答案和解析>>
科目: 来源: 题型:
某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)某课外兴趣小组利用该残渣制取Fe2O3粉末的实验流程如下:(说明:流程中向黄色溶液中加入MgO的目的是调节溶液的酸碱性,使Fe3+ 生成沉淀而Mg2+不沉淀)
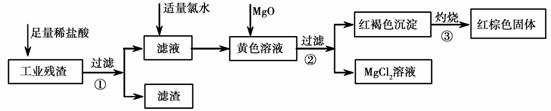
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A.置换反应 B.化合反应 C.分解反应 D.复分解反应 E.氧化还原反应
(2)加入适量氯水的作用是 ;
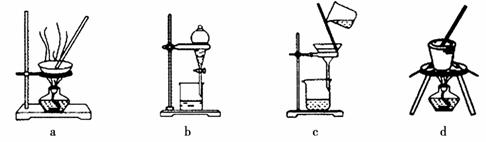
(3)写出灼烧红褐色沉淀时发生反应的化学方程式 。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。
(4)若向黄色溶液中加入过滤①后的滤渣发生反应的离子方程式为 。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中, 。(请补充完整实验操作、现象、结论)
查看答案和解析>>
科目: 来源: 题型:
通常用饱和NaHCO3溶液除去混在CO2中的少量HCl气体,其反应的离子方程式为 ;不能用NaOH溶液的原因是
(用离子方程式表示);也不能用Na2CO3溶液吸收的原因是) (用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
目前,汽车尾气已成为许多大城市空气的主要污染。汽车尾气中含有CO、NO等多种污染物。
(1)汽车燃料中一般不含氮,尾气中所含的NO产生的原因是 , 化学方程式为 。
(2)治理汽车尾气中NO和CO的一种方法是:在汽车的排气管上装上一个催化转化装置,使NO和CO反应,生成CO2和 N2。反应的化学方程式为 。
(3)下列措施中,能减少或控制汽车尾气污染有效且可行的是 。
① 制定严格的尾气排放标准,并严格执行。 ② 开发清洁能源,如氢能汽车、太阳能汽车等。 ③ 市民出行带防毒面具。 ④ 市民大量移居城市郊区。
查看答案和解析>>
科目: 来源: 题型:
含氯化镁和氯化铝的混合溶液200 mL,其中c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为
A.40 mL B.72 mL C.80 mL D.128 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com