
科目: 来源: 题型:
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl====Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
A.正极反应:Ag+Cl--e-====AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
查看答案和解析>>
科目: 来源: 题型:
如图所示,杠杆AB两端分别持有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入较浓的硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑两球的浮力变化)( )

A.当杠杆为绝 缘体时,A端高、B端低;为导体时,A端低、B端高
缘体时,A端高、B端低;为导体时,A端低、B端高
B.当杠杆为绝缘体时,A端低、B端高;为导体时,A端高、B端低
C.当杠杆为导体或绝缘体时,均为A端高B端低
D.当杠杆为导体或绝缘体时,均为A端低B端高
查看答案和解析>>
科目: 来源: 题型:
有关如图所示原电池的叙述 ,正确的是( )
,正确的是( )
(盐桥中装有含琼胶的KCl饱和溶液)
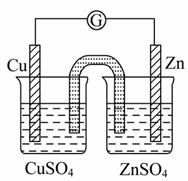
A.铜片上有气泡逸出
B.取出盐桥后,检流计依然发生偏转
C.反应中,盐桥中的K+会移 向CuSO4溶液
向CuSO4溶液
D.反应前后铜片质量不改变
查看答案和解析>>
科目: 来源: 题型:
一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取的措施是( )
A.加入少量稀氢氧化 钠溶液
钠溶液
B.加入少量CH3COONa固体
C.加入少量NH4HSO4固体
D.加入少量CuSO4溶液
查看答案和解析>>
科目: 来源: 题型:
下列四组原电池放电后,电解质溶液质量增加,且在正极上有单质生成的是( )
A.Cu、Ag、AgNO3溶液  B.Zn、Cu、稀硫酸
B.Zn、Cu、稀硫酸
C.Fe、Zn、CuSO4溶液 D.Fe、C、Fe2(SO4)3溶液
查看答案和解析>>
科目: 来源: 题型:
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2 (g)+3H2 (g)2NH3 (g) ΔH=-92.4 kJ·mol-1
一种工业合成氨的简易流程图如下:
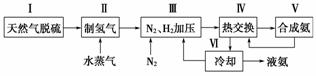
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式: __________________________________________________________。
(2)步骤Ⅱ中制氢气原理如下:
①CH4(g)+H2O(g)CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g)CO2(g)+H2(g) ΔH=-41.2 kJ· mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是________。
a.升高温度 b.增大水蒸气浓度
c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO转化率为________。
(3)图1表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:________。
(4)依据温度对合成氨反应的影响,在图2坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。

(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________。简述本流程中提高合成氨原料总转化率的方法:__________________________________________________________
__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
2NO(g) +O2(g)2NO2(g) 。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
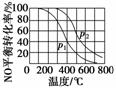
①比较p1、p2的大小关系________。
②随温度升高,该反应平衡常数变化的趋势是________。
(2)[2014·广东理综,31(2)(3)(4)]用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
① 1/4CaSO4(s)+CO(g)1/4CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
② CaSO4(s)+CO(g)CaO(s)+CO2(g) +SO2(g) ΔH2=+210.5 kJ·mol-1
③ CO(g)1/2C(s)+1/2CO2(g) ΔH3=-86.2 kJ·mol-1
①反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见下图,结合各反应的ΔH,归纳lgK~T曲线变化规律:

a.__________________________________________________________;
b.__________________________________________________________。
②向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900 ℃达到平衡,c平衡(CO)=8.0×10-5 mol·L-1,计算CO的转化率(忽略副反应,结果保留两位有效数字)。
③为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入________。
查看答案和解析>>
科目: 来源: 题型:
已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=________,ΔH________0(填“<”、“>”或“=”);
(2)830℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,如反应初始6 s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=________ mol·L-1,C的物质的量为________mol;反应经一段时间,达到平衡时A的转化率为________,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为________;
(3)判断该反应是否达到平衡的依据为________(填正确选项前的字母);
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
(4)1 200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为________。
查看答案和解析>>
科目: 来源: 题型:
利用醋酸二氨合铜[Cu(NH3)2Ac]溶液吸收CO,能达到保护环境和能源再利用的目的,反应方程式为Cu(NH3)2Ac+CO+NH3[Cu(NH3)3]Ac·CO。已知该反应的化学平衡常数与温度的关系如表所示:
| 温度/℃ | 15 | 50 | 100 |
| 化学平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是(双选)( )
A.上述正反应为放热反应
B.15℃时,反应[Cu(NH3)]Ac·COCu(NH3)2Ac+CO+NH3的平衡常数为0.5
C.保持其他条件不变,减小压强,CO的转化率减小
D.醋酸二氨合铜溶液的浓度大小对CO的吸收没有影响
查看答案和解析>>
科目: 来源: 题型:
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5(g)4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据如表所示:
| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是(双选)( )
A.500 s内N2O5的分解速率为2.96×10-3 mol·L-1·s-1
B.T1温度下的平衡常数K1=125,1 000 s时N2O5的转化率为50%
C.其他条件不变时,T2温度下反应到1 000 s时测得N2O5(g)的浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1<T3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com