
科目: 来源: 题型:
下列四种元素中,其单质氧化性最强的是( )
A.原子含有未成对电子最多的第二周期元素 B.位于周期表中第三周期ⅢA族的元素
C.原子最外层电子排布为2s22p4的元素 D.原子最外层电子排布为3s23p3的元素
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是 ( )
A.p区元素全部都是主族元素
B.稀有气体的原子的电子排布最外层都是以P6结束
C.主族元素的原子核外电子最后填入的能级是s能级或p能级
D.核外电子排布相同的微粒,一定具有相同的化学性质
查看答案和解析>>
科目: 来源: 题型:
下列各项叙述中,正确的是( )
A.电子层序数越大,s原子轨道的半径越大,形状发生明显的变化
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.电负性的大小可以作为判断金属性和非金属性强弱的尺度
D.原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目: 来源: 题型:
下列关于价电子构型3s23p4的描述正确的是( )
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.可以与H2化合生成液态化合物
D.其电子排布图为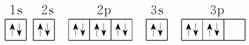
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是( )
A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
D.某基态原子错误的核外电子排布图为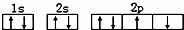 该排布图违背了泡利原理
该排布图违背了泡利原理
查看答案和解析>>
科目: 来源: 题型:
在以下性质的比较中,正确的是
A.微粒半径:O2-<F-<Na+<Li+ B.第一电离能:C < N < O
C.分子中的键角:CH4>H2O>CO2 D.共价键的键能:C-C < C=C < C≡C
查看答案和解析>>
科目: 来源: 题型:
25 ℃时,KHS溶液里存在着下列平衡:
①HS-+H2O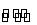 OH-+H2S
OH-+H2S
②HS-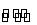 H++S2-
H++S2-
(1)_______是电离平 衡,________是水解平衡。
衡,________是水解平衡。
(2)当向其中加入CuSO4溶液时,生成了CuS沉淀,则电离平衡向________移动,水解平衡向_________移动,[H+]变________。(填“大”或“小”)
(3)当向其中加入NaOH固体时,[S2-]变_____________。(填“大”或“小”)
(4)若将溶液加热至沸腾,[OH-][H+]将变__________。(填“大”或“小”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com