
科目: 来源: 题型:
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3 mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下图为H2CO3在加入强酸或强碱溶液溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:
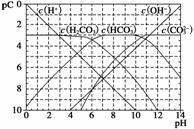
(1)在人体血液中,HCO 能起到使人体血液pH保持在7.35~7.45的作用。
能起到使人体血液pH保持在7.35~7.45的作用。
①请用电解质溶液中的平衡解释:__________________(用离子方程式表示)。
②正常人体血液中,HCO 的水解程度________电离程度(填“<”、“>”或“=”)。
的水解程度________电离程度(填“<”、“>”或“=”)。
③pH=7.00的血液中,c(H2CO3)________c(HCO )(填“<”、“>”或“=”)。
)(填“<”、“>”或“=”)。
(2)H2CO3一级电离平衡常数的数值Ka1≈________。
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO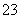 不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1、c(CO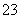 )=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
)=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
查看答案和解析>>
科目: 来源: 题型:
碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3HCO +H+的平衡常数K1=________。(已知:10-5.60=2.5×10-6)
+H+的平衡常数K1=________。(已知:10-5.60=2.5×10-6)
查看答案和解析>>
科目: 来源: 题型:
在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH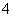 )=c(Cl-),则溶液显__________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=______________________________________________________。
)=c(Cl-),则溶液显__________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
25 ℃时,0.01 mol·L-1两种弱酸溶液的pH如表。下列说法正确的是( )
| 弱酸 | CH3COOH | HCN |
| pH | 3.4 | 5.6 |
A.相同pH的两种酸溶液中,CH3COOH溶液中水电离的c(H+)较大
B.物质的量浓度相同的CH3COONa与NaCN溶液中,CH3COONa溶液的pH较大
C.等体积、相同pH的两种酸溶液,分别滴加NaOH溶液至恰好中和,消耗等量的NaOH
D.HCN的电离平衡常数(Ka)与CN-的水解平衡常数(K)存在如下关系:Ka·K=Kw
查看答案和解析>>
科目: 来源: 题型:
化工生产中常用MnS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+Mn2+(aq),下列说法错误的是(双选)( )
A.MnS的Ksp比CuS的Ksp小
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=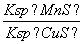
查看答案和解析>>
科目: 来源: 题型:
已知温度T时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=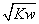 mol·L-1
mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目: 来源: 题型:
不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示。下列有关说法中正确的是( )
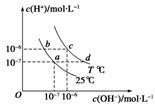
A.若从a点到c点,可采用在水中加入酸的方法
B.b点对应的醋酸中由水电离的c(H+)=10-6 mol·L-1
C.c点对应溶液的Kw大于d点对应溶液的Kw
D.T ℃时,0.05 mol·L-1的Ba(OH)2溶液的pH=11
查看答案和解析>>
科目: 来源: 题型:
25 ℃时,H2SO3HSO +H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=______mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
室温下,0.1 mol·L-1的硫化钠溶液和0.1 mol·L-1的碳酸钠溶液,碱性更强的是__________,其原因是___________________________________________________。
已知:H2S:Ki1=1.3×10-7 Ki2=7.1×10-15
H2CO3:Ki1=4.3×10-7 Ki2=5.6×10-11
查看答案和解析>>
科目: 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化曲线如下图所示。下列说法错误的是( )
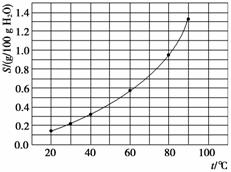
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com