
科目: 来源: 题型:
室温时,将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是( )
A.若pH>7,则一定是c1V1=c2V2
B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.当pH=7时,若V1=V2,则一定是c2>c1
D.若V1=V2,c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目: 来源: 题型:
常温下,下列有关醋酸溶液的叙述中不正确的是( )
A.pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
C.将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)减小
D.等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14
查看答案和解析>>
科目: 来源: 题型:
下列5种混合溶液,分别由0.1 mol·L-1的两种溶液等体积混合而成:①CH3COONa与NaHSO4,②CH3COONa与NaOH,③CH3COONa与NaCl,④CH3COONa与NaHCO3,⑤CH3COONa与NaHSO3。下列各项排序正确的是( )
A.pH:②>④>⑤>③>①
B.c(CH3COOH):①>③>⑤>④>②
C.c(CH3COO-):②>③>④>⑤>①
D.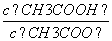 :①>⑤>③>④>②
:①>⑤>③>④>②
查看答案和解析>>
科目: 来源: 题型:
常温下a mol·L-1稀氨水和b mol·L-1稀盐酸等体积混合,对混合后溶液判断一定正确的是( )
A.若a=b,则c(NH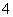 )=c(Cl-) B.若a>b,则c(NH
)=c(Cl-) B.若a>b,则c(NH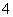 )>c(Cl-)
)>c(Cl-)
C.若a>b,则c(OH-)>c(H+) D.若a<b,则c(OH-)<c(H+)
查看答案和解析>>
科目: 来源: 题型:
已知相同温度下电离常数K(HF)>K(HCN),在物质的量浓度均为0.1 mol·L-1的NaCN和NaF混合溶液中,下列排序正确的是( )
A.c(OH-)>c(HF)>c(HCN)>c(H+)
B.c(OH-)>c(CN-)>c(F-)>c(H+)
C.c(OH-)>c(F-)>c(CN-)>c(H+)
D.c(F-)>c(OH-)>c(HCN)>c(HF)
查看答案和解析>>
科目: 来源: 题型:
室温下,下列溶液中粒子浓度关系正确的是( )
A.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
B.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O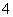 )+2c(H2C2O4)
)+2c(H2C2O4)
C.Na2CO3溶液:c(Na+)+c(H+)=2c(CO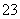 )+c(OH-)
)+c(OH-)
D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
查看答案和解析>>
科目: 来源: 题型:
25℃时,现有0.1 mol·L-1的氨水。请回答下列问题:
(1)为了证明一水合氨(NH3·H2O)是弱电解质,常温下,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、0.1 mol·L-1 NH4Cl溶液,NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
①甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?________(填“是”或“否”),请说明理由:__________________________________________________________
__________________________________________________________。
②乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出pH为b,若要确认NH3·H2O是弱电解质,则a、b应满足关系:________________(用等式或不等式表示)。
③丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞试剂,显粉红色,再加入少量NH4Cl晶体,颜色变________(填“深”或“浅”)。你认为这一方法能否证明NH3·H2O是弱电解质?________(填“能”或“否”),并说明原因:__________________________________________________________
__________________________________________________________。
(2)若向氨水中加入少量硫酸铵固体,此时溶液中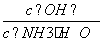 ________(填“增大”、“减小”或“不变”)。
________(填“增大”、“减小”或“不变”)。
(3)若向氨水中加入稀硫酸,二者恰好完全反应后所得溶液的pH________7(填“>”、“<”或“=”),用离子方程式解释原因:__________________________________________________________
__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
一条件下,CH3COOH溶液中存在电离平衡:
CH3COOHCH3COO-+H+ ΔH>0
(1)下列方法中,可以使0.10 mol·L-1 CH3COOH溶液中CH3COOH电离程度增大的是________。
a.加入少量0.10 mol·L-1稀盐酸 b.加热
c.加水稀释至0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1 NaOH溶液
(2)25℃时,醋酸的电离平衡常数为1.75×10-5。现有:
①0.10 mol·L-1 CH3COOH溶液 ②0.001 mol·L-1 CH3COOH溶液
①和②中c(H+)之比为________。[提示:进行简化计算,平衡时c(CH3COOH)可用起始浓度代替,水电离出的c(H+)、c(OH-)忽略不计]
查看答案和解析>>
科目: 来源: 题型:
HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是(双选)( )
A.0.1 mol·L-1 HA溶液中c(H+)=c(OH-)+c(A-)
B.0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液混合至溶液呈中性:c(Na+)=c(A-)
C.0.1 mol·L-1 NaA溶液中c(Na+)>c(OH-)>c(A-)>c(H+)
D.0.1 mol·L-1 HA溶液中加入少量NaA固体,HA的电离常数减小
查看答案和解析>>
科目: 来源: 题型:
常温下,有下列四种溶液:
| ① | ② | ③ | ④ |
| 0.1 mol·L-1 NaOH溶液 | pH=11 NaOH溶液 | 0.1 mol·L-1 CH3COOH溶液 | pH=3 CH3COOH溶液 |
下列说法正确的是(双选)( )
A.由水电离出的c(H+):③>①
B.③稀释到原来的100倍后,pH与④相同
C.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH)
D.②④混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com