
科目: 来源: 题型:
下列实验事实不能证明醋酸是弱电解质的是( )
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1 mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.在相同条件下,醋酸溶液的导电性比盐酸的弱
查看答案和解析>>
科目: 来源: 题型:
20℃时,H2S的饱和溶液1 L,浓度约0.1 mol·L-1,其电离方程式为:第一步:H2S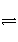
 H++HS-;第二步:HS-
H++HS-;第二步:HS-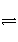
 H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
①加入适量NaOH固体 ②加入适量水 ③通入适量SO2 ④加入适量CuSO4固体
A.①④ B.②④ C.②③ D.①③
查看答案和解析>>
科目: 来源: 题型:
将1 mol冰醋酸加入到一定量的蒸馏水中最终得到1 L溶液。下列各项中,表征已达到电离平衡状态的是( )
A.醋酸的浓度达到1 mol·L-1
B.[H+]的浓度达到0.5 mol·L-1
C.[CH3COOH]、[CH3COO-]、[H+]均为0.5 mol·L-1
D.醋酸分子电离成离子的速率和离子重新结合成分子的速率相等
查看答案和解析>>
科目: 来源: 题型:
已知下面三个数据:7.2×10-4 mol·L-1、4.6×10-4 mol·L-1、4.9×10-10 mol·L-1分别是三种酸的电离平衡常数,若已知这些酸可发生如下反应:
①NaCN+HNO2===HCN+NaNO2,
②NaCN+HF===HCN+NaF,
③NaNO2+HF===HNO2+NaF。
由此可判断下列叙述中,不正确的是( )
A.HF的电离平衡常数为7.2×10-4
B.HNO2的电离平衡常数为4.9×10-10
C.根据①③两个反应即可知三种酸的相对强弱
D.HNO2的电离平衡常数比HCN大,比HF小
查看答案和解析>>
科目: 来源: 题型:
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH(固体) ②H2O ③HCl ④CH3COONa(固体)
A.②④ B.①④ C.②③ D.①③
查看答案和解析>>
科目: 来源: 题型:
下列对氨水溶液中存在的电离平衡NH3·H2O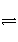
 NH
NH +OH-叙述正确的是( )
+OH-叙述正确的是( )
A.加水后,溶液中n(OH-)增大
B.加入少量浓盐酸,溶液中[OH-]增大
C.加入少量浓NaOH溶液,电离平衡正向移动
D.加入少量NH4Cl固体,溶液中[NH ]减少
]减少
查看答案和解析>>
科目: 来源: 题型:
在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是( )
A.加热
B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸
D.加入少量的1 mol·L-1的NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH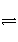
 CH3COO-+H+。要使[H+]/[CH3COOH]值增大,可采取措施( )
CH3COO-+H+。要使[H+]/[CH3COOH]值增大,可采取措施( )
A.加少量烧碱溶液 B.降低温度
C.加少量冰醋酸 D.加水
查看答案和解析>>
科目: 来源: 题型:
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH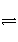
 CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1HCl溶液,溶液中[H+]减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com