
科目: 来源: 题型:
下列叙述正确的是( )
A.有单质参加或单质生成的化学反应一定是氧化还原反应
B.生成物只有一种的化学反应不一定是化合反应
C.生成阳离子的反应一定是氧化反应
D.有电解质参加的化学反应一定可以用离子方程式表示
查看答案和解析>>
科目: 来源: 题型:
高氯酸铵(NH4ClO4)加热至483 K时,可完全分解成N2、Cl2、O2和H2O,则反应中氧化产物与还原产物的物质的量之比是( )
A.1∶1 B.1∶3 C.2∶1 D.3∶1
查看答案和解析>>
科目: 来源: 题型:
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是 ( )
A.Na+、Ba2+、Cl、SO42- B. Ca2+、HCO3、C1、K+
C.MnO4、K+、I、H+ D. H+ 、Cl 、Na+ 、CO32
查看答案和解析>>
科目: 来源: 题型:
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是( )。
A.Na2O2在上述反应中既作氧化剂又作还原剂
B.Na2FeO4既是氧化产物又是还原产物
C.Na2FeO4处理水时,既能杀菌,又能在处理水时产生胶体净水
D.2 mol FeSO4发生反应时,共有8 mol电子发生转移
查看答案和解析>>
科目: 来源: 题型:
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为____________。
(2)写出该反应的化学方程式_________________________________________________。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是
。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有__________________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-===2H++O2↑ 还原反应:MnO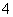 +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
(1)写出该氧化还原反应的离子方程式:________________________________________。
(2)该反应中氧化剂是________,被氧化的元素是________;若有0.5 mol H2O2参加此反应,则转移电子个数为________。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为
;这时若有0.5 mol H2O2发生分解,则转移电子个数为________。
查看答案和解析>>
科目: 来源: 题型:
配平下列氧化还原反应方程式,并标明反应④电子转移的方向和数目。
① H2S+
H2S+ H2SO3——
H2SO3—— S↓+
S↓+ H2O
H2O
氧化产物是_________,还原产物是__________,二者质量比是________。
② Cl2+
Cl2+ KOH——
KOH—— KCl+
KCl+ KClO3+
KClO3+ H2O
H2O
氧化剂是________,还原剂是________,二者物质的量之比是__________。
③ KClO3+
KClO3+ HCl——
HCl—— KCl+
KCl+ Cl2↑+
Cl2↑+ H2O
H2O
HCl的作用是________,被还原的元素是__________,当反应过程中有3 mol电子转移时,可产生氯气________mol。
④ KIx+
KIx+ Cl2+
Cl2+ H2O——
H2O—— KCl+
KCl+ HIO3+
HIO3+ HCl
HCl
若KIx与Cl2的化学计量数之比为1∶8,则x=____________。
查看答案和解析>>
科目: 来源: 题型:
与铁相似,金属锡能溶于盐酸生成氯化亚锡,氯化亚锡又能被氯化铁氧化为氯化锡。则下列有关微粒氧化、还原能力的比较中,正确的是( )
A.氧化能力:Sn4+<Sn2+ B.氧化能力:Fe3+<Sn4+
C.还原能力:Fe2+<Sn2+ D.还原能力:Fe<Sn
查看答案和解析>>
科目: 来源: 题型:
臭氧具有强氧化性,可使湿润的碘化钾淀粉试纸变蓝,有关反应如下:
O3+2KI+H2O===2KOH+I2+O2 ,下列对于此反应的说法正确的是( )
A.反应中,O3是氧化剂,H2O和KI是还原剂
B.氧化产物I2与还原产物O2的物质的量之比为1∶1
C.在反应中,1 mol O3得2 mol电子
D.由此反应可知,氧化性强弱顺序为:O3>I2>O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com