
科目: 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) 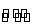 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
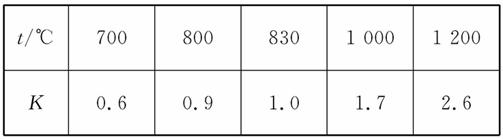
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________。
(2)能判断该反应是否达到化学平衡状态的依据是_____________________。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.[CO2]=[CO]
(3)某温度下,平衡浓度符合:[CO2]·[H2]=[CO]·[H2O],试判断此时的温度为__________℃。
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,将2 mol A和2 mol B两种气体混合放入体积为2 L的 密闭刚性容器中,发生反应:3A(g)+B(g)
密闭刚性容器中,发生反应:3A(g)+B(g)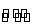 xC(g)+2D(g)
xC(g)+2D(g)
2 min末反应达到平衡,生成0.8 mol D,并测得C的浓度为0.4 mol·L-1,下列说法正确的是( )
D,并测得C的浓度为0.4 mol·L-1,下列说法正确的是( )
A.x的值为1
B.A的转化率为40%
C.此温度下该反应的平衡常数K等于0.5
D.A和B的平衡转化率相等
查看答案和解析>>
科目: 来源: 题型:
恒温(1 100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g) 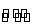 Na2S(s)+
Na2S(s)+
4H2O(l),下列说法中正确的是( )
A.该平衡常数表达式为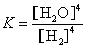
B.容器内气体的质量或压强保持不变,均可说明该反应已达到平衡状态
C.若Na2SO4足量,改变起始充入H2的浓度,则达到平衡时的H2转化率不变
D.若初始时投入2.84 g Na2SO4与一定量H2,反应达到平衡时容器内固体共有2.264 g,则Na2SO4的转化率为25%
查看答案和解析>>
科目: 来源: 题型:
在一密闭容器中,用等物质的量的A和B发生如 下反应:A(g)+2B(g)
下反应:A(g)+2B(g)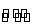
2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则此时A的转化率为( )
A.40% B.50% C.60% D.70%
查看答案和解析>>
科目: 来源: 题型:
已知反应①Fe(s)+CO2(g)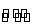 FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)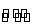 FeO(s)+H
FeO(s)+H 2(g)的平衡常数为K2。 反应CO2(g)+H2(g)
2(g)的平衡常数为K2。 反应CO2(g)+H2(g) 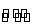 CO(g)+H2O(g)的平衡常数K为( )
CO(g)+H2O(g)的平衡常数K为( )
A.K1+K2 B.K1-K2 C.K1· K2 D.K1/K2
K2 D.K1/K2
查看答案和解析>>
科目: 来源: 题型:
能够充分说明在恒温恒容下的密闭容器中,反应2SO2(g)+O2(g) 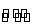
2SO3(g)已达平衡状态的标志是( )
A.容器中SO2、O2、SO3的物质的量之比为2∶1∶2
B.SO2和SO3的物质的量浓度相等
C.反应容器内压强不随时间变化而变化
D.单位时间内生成2 mol SO3的同时生成1 mol O2
查看答案和解析>>
科目: 来源: 题型:
下列平衡常数K表示反应进行的程度,K越大,表示反应进行得 越彻底。关于化学平衡常数的叙述不正确的是( )
越彻底。关于化学平衡常数的叙述不正确的是( )
A.温度一定,一个化学反应的平衡常数不变
B.两种物质反应,不管怎样书写化学方程式,平衡常数不变
C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数
D.从平衡常数的大小可以推断一个反应进行的程度
查看答案和解析>>
科目: 来源: 题型:
甲醛是室内污染的重要有害物质,碘量滴定法是测定甲醛的化学方法之一,其原理是在碱性介质(NaOH)中,碘转化为次碘酸钠和碘化钠,次碘酸钠将溶液中游离的甲醛氧化为甲酸钠;经适当酸化后,剩余的次碘酸钠与碘化钠又生成碘;以淀粉为指示剂,用硫代硫酸钠标准溶液滴定。
上述过程中涉及的化学反应的离子方程式依次为
(1)I2+2OH-===IO-+I-+H2O;
(2)________________________________________________________________________;
(3)________________________________________________________________________;
(4)I2+2S2O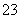 ===S4O
===S4O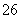 +2I-。
+2I-。
查看答案和解析>>
科目: 来源: 题型:
将FeSO4溶液的pH调节至7左右,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是________。
查看答案和解析>>
科目: 来源: 题型:
在盛有10 mL 1.0 mol·L-1的碘水的试管中,通入足量Cl2完全反应后,共转移了0.1 mol电子。写出该反应的化学方程式:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com