
科目: 来源: 题型:
在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)  CO(g)+H2O(g),其
CO(g)+H2O(g),其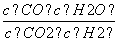 =K,K被称为化学平衡常数,其中K和温度的关系如下表:
=K,K被称为化学平衡常数,其中K和温度的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1. 0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是( )
A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1000 ℃时的反应速率比700 ℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目: 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )。
A.溴水中有Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B.加催化剂,使N2和H2在一定条件下转化为NH3
C.反应CO(g)+NO2(g)  CO2(g)+NO(g) ΔH<0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g) ΔH<0,达平衡后,升高温度体系颜色变深
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目: 来源: 题型:
FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某化学研究小组为探究在酒精喷灯加热条件下FeSO4分解的气体产物,进行了一系列实验。已知SO3的熔点是16.8 ℃,沸点是44.8 ℃。
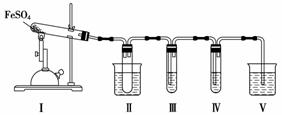
请回答下列问题:
(1)装置Ⅱ的试管中不装任何试剂,其作用是__________________________,试管浸泡在50 ℃的水中,其目的是____________________。
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验中气体产物的成分。请完成实验设计,填写检验试剂、预期现象与结论。限选试剂:3 mol·L-1 H2SO4溶液、6 mol·L-1 NaOH溶液、0.5 mol·L-1 BaCl2溶液、0.5 mol·L-1 Ba(NO3)2溶液、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水。
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中装有______________ | 产生大量白色沉淀,证明气体产物中含有SO3 |
| 装置Ⅳ的试管中装有____________ |
(3)装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是__________。
(4)已知在过量的FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
①甲同学推测该反应的还原产物有两种可能:a.Cl2、b:Cl-。
乙同学结合甲同学的推测,认为其中一种可能可以排除,你认为可以排除的是哪种可能,并用简要的文字和离子方程式说明理由:________________。
②上述反应的离子方程式为__________________。
③为检验上述反应中的还原产物,请选择所需实验步骤,并按先后次序排列:__________(填序号)。
A.取一支试管,加入上述反应后的溶液少许
B.加入过量Ba(NO3)2溶液,出现白色沉淀
C.过滤;取滤液加入硝酸酸化的AgNO3溶液,出现白色沉淀
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其他还原性离子)进行了检测,其中三次检测结果如表所示:
| 检测序号 | 溶液中检测出的电解质溶液组合 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、AlCl3、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
则下列说法合理的是( )
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验是否存在SO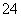 ,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
D.为了检验是否存在CO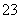 ,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
查看答案和解析>>
科目: 来源: 题型:
根据下列实验内容得出的结论正确的是( )
| 选项 | 实验内容 | 结论 |
| A | 某物质的水溶液使红色石蕊试纸变蓝 | 该物质一定是碱 |
| B | 某气体能使湿润的淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| C | 向某物质的水溶液中加入盐酸,产生无色无味气体 | 该溶液中一定含有碳酸根离子 |
| D | 向铁和稀硝酸反应后的溶液中滴入KSCN溶液,溶液显血红色 | 反应后溶液中肯定有Fe3+,可能还有Fe2+ |
查看答案和解析>>
科目: 来源: 题型:
为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH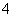 、Fe2+、SO
、Fe2+、SO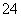 与H2O,下列实验叙述中不正确的是( )
与H2O,下列实验叙述中不正确的是( )
A.取少量硫酸亚铁铵晶体于试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B.取少量硫酸亚铁铵晶体溶于水,得到浅绿色溶液,滴入2滴KSCN溶液,溶液不显血红色,再滴入几滴新制氯水,溶液变为血红色,则可证明晶体的成分中含有Fe2+
C.取少量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO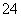
D.取少量硫酸亚铁铵晶体溶于水,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,若试纸变蓝,则可证明晶体的成分中含有NH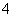
查看答案和解析>>
科目: 来源: 题型:
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。经小组讨论并验证无色气体为O2,其验证方法是________________________________________________________________________。

(2)[2013·海南17(1)改编]BaCl2·xH2O中结晶水数目可通过重量法来确定;①称取样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;②过滤并洗涤沉淀;③……
在操作②中,需要先后用稀硫酸和________洗涤沉淀;检验沉淀中氯离子是否洗净的方法是________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下列实验可实现鉴别目的的是( )
A.用KOH溶液鉴别SO3(g)和SO2
B.用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和CH3COONa溶液
D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液
查看答案和解析>>
科目: 来源: 题型:
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:__________________。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是________________________________。
(3)吸收液吸收SO2的过程中,pH随n(SO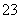 )∶n(HSO
)∶n(HSO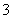 )变化关系如下表:
)变化关系如下表:
| n(SO | 91∶9 | 1∶1 | 1∶91 |
| pH | 8.2 | 7.2 | 6.2 |
上表判断NaHSO3溶液显________性,用化学平衡原理解释:______________________________。
查看答案和解析>>
科目: 来源: 题型:
化学与社会、环境等密切相关。下列说法错误的是( )
A.“低碳经济”是指减少对化石燃料的依赖,达到低污染、低排放的模式
B.“低碳生活”倡导生活中耗用能量尽量减少,从而减少CO2的排放
C.所有垃圾都可以采用露天焚烧或深埋的方法处理
D.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com