
科目: 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属,且与R同周期。下列叙述正确的是( )
A.离子半径大小:Y2->R3+>M2-
B.Z与M的气态氢化物的稳定性:Z>M
C.将YM2通入溶有Z的气态氢化物的BaCl2溶液中没有白色沉淀产生
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
查看答案和解析>>
科目: 来源: 题型:
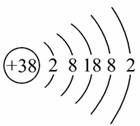
以锶原子作钟摆的钟是世界上最精确的钟。锶元素(元素符号为Sr)的原子结构示意图如图所示,下列说法正确的是( )
A.氮化锶的化学式为Sr2N3 B.锶可与水反应生成O2
C.氢氧化锶为弱碱 D.第一电离能:Sr<Ca
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法不正确的是( )
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE所含化学键的类型不同
查看答案和解析>>
科目: 来源: 题型:
在周期表主族元素中,甲元素与乙、丙、丁三种元素紧密相邻。这四种元素原子的最外层电子数之和为20;甲、丁的原子序数之和比乙、丙的原子序数之和大10;乙的原子序数小于丙。下列判断中不正确的是( )
A.甲的某种单质与丙的单质均可形成正四面体空间结构
B.四种原子半径:丙>乙>甲>丁
C.甲、乙、丙、丁四种单质的熔点最低的是乙
D.乙的氢化物与丁的氢化物能相互反应
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应水化物的酸性从左到右依次增强
D.第2周期元素随族序数的递增其最高化合价也递增
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z是元素周期表中的三种短周期元素,三者的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
| X | ||
| Z | Y |
A.Z一定是活泼的金属元素
B.Y不存在最高价氧化物
C.1 mol Y的单质溶于足量水时,反应转移的电子为1 mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
查看答案和解析>>
科目: 来源: 题型:
原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1。下列有关X的说法中正确的是( )
A.X位于元素周期表中第2周期ⅤA族
B.X元素有-3、+5两种化合价
C.X元素在元素周期表中的族序数肯定为奇数
D.X元素最高价氧化物对应的水化物可以表示为H3XO4
查看答案和解析>>
科目: 来源: 题型:
2012年8月7日“好奇号”传回火星第一张彩照,火星岩石中富含铁而使其表面呈红色,下列有关铁的说法中正确的是(已知Fe是26号元素)( )
A.铁元素位于周期表中第4周期第ⅦB族
B.57Fe和55Fe互为同素异形体
C.铁比铝更易被腐蚀,说明铁比铝活泼
D.铁原子在化学反应中可失去2个或3个电子
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.实验室有一瓶失去标签的某白色固体,已知其成分可能是碳酸或亚硫酸的钠盐或钾盐,且其成分单一。现某化学小组通过如下步骤来确定其成分:
(1)阳离子的确定:
实验方法及现象: 。
结论:此白色固体是钠盐。
(2)阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
Ⅱ.确认其成分后,由于某些原因,此白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤Ⅰ 称取样品1.000 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤Ⅲ所发生反应的离子方程式 。
(2)在配制0.01 mol·L-1KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量 (填“偏大”“偏小”或“无影响”)。
(3)滴定结果如下表所示:
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
则该变质固体中X的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
现有常温条件下甲、乙、丙三种溶液,甲为
0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的HCl溶液,丙为0.1 mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH= ;
(2)丙溶液中存在的电离平衡为
(用电离方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为 ;
(4)某同学用甲溶液分别滴定20.00 mL乙溶液和20.00 mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题:
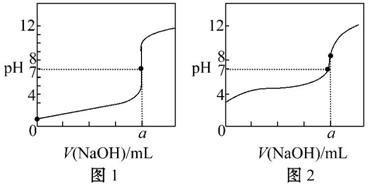
①甲溶液滴定丙溶液的曲线是 (填“图1”或“图2”);
②a= mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com