
科目: 来源: 题型:
下列说法正确的是( )
A.在化学反应中发生物质变化的同时,不一定发生能量变化
B.ΔH>0表示放热反应,ΔH<0表示吸热反应
C.ΔH的大小与热化学反应方程式中化学计量数无关
D.生成物释放的总能量大于反应物吸收的总能量时,ΔH<0
查看答案和解析>>
科目: 来源: 题型:
在研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及其能量变化,据此判断以下叙述中错误的是( )
A.化学反应的实质是旧化学键断裂和新化学键的形成
B.所有的化学变化一定遵循质量守恒和能量守恒
C.在化学反应中,破坏旧化学键吸收的能量大于形成新化学键释放的能量时,该反应是放热反应
D.化学键的变化必然会引起能量变化,所以能量变化也一定会引起化学变化
查看答案和解析>>
科目: 来源: 题型:
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: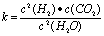 它所对应的化学反应为:
它所对应的化学反应为:
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填选项字母)。
A. =0.8 mol·L-1 B. =1.4 mol·L-1 C. <1.4 mol·L-1 D. >1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平衡时各气体的体积分数与甲容器完全相同的是 (填选项字母)。
A. 0.6 mol 1.0 mol 0.5 mol 1.0 mol B. 0.6 mol 2.0 mol 0 mol 0 mol
C. 1.0 mol 2.0 mol 1.0 mol 2.0 mol D. 0.25 mol 0.5 mol 0.75 mol 1.5 mol
(3)将燃煤废气中的CO2转化为甲醚的反应原理为:
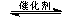 2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S 0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。
若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜
g。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.实验室常见的几种气体发生装置如图A、B、C所示:
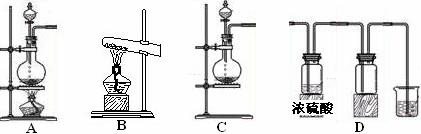
(1) 实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为
。
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是
_____________(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可以是下列气体中的________。
①CO2 ②NO ③Cl2 ④H2 ⑤HCl
其中在D装置中连接小烧杯的目的是 。
Ⅱ.某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
(4)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3 ,钴的化合价为________,制备X的化学方程式为
已知:X的化学式类似下列化学式
氢氧化二氨合银:Ag(NH3)2OH 、硫酸四氨合铜:Cu(NH3)4SO4
(5)氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。
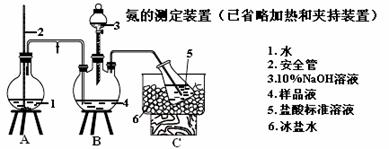
①盛放5(盐酸标准溶液)的仪器名称
②装置中安全管的作用原理是
③样品中氨的质量分数表达式为
查看答案和解析>>
科目: 来源: 题型:
以乙炔或苯为原料可合成有机酸H2MA,并进一步合成高分子化合物PMLA。
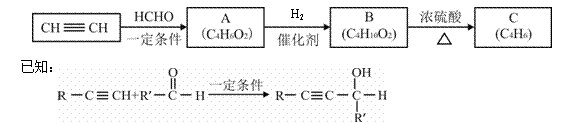 I.用乙炔等合成烃C。
I.用乙炔等合成烃C。
(1)A分子中的官能团名称是 、
(2)A的结构简式是
A的一种同分异构体属于乙酸酯,其结构简式是 。
(3)B转化为C的化学方程式是 ;
其反应类型是 反应。
II.用烃C或苯合成PMLA的路线如下。

已知:

(4)1 mol有机物H与足量NaHCO3溶液反应生成标准状况下的CO2 44.8 L,H有顺反异构,其反式结构简式是
(5)E的结构简式是
(6)G与NaOH溶液在加热条件下反应的化学方程式是
(7)H的核磁共振氢谱呈现 个吸收峰。
(8)聚酯PMLA有多种结构,写出由H2MA制PMLA的化学方程式(任写一种)
查看答案和解析>>
科目: 来源: 题型:
四种常见的短周期非金属元素在周期 表中的相对
表中的相对 位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
| 甲 | 乙 | |
| 丙 | 丁 |
请用化学用语回答:
(1)丙在元素周期表中的位置是 。
(2)丁单质的电子式是 。
(3)乙的两种常见单质分别是 、 。
(4)甲、乙、丙、丁的气态氢化物水溶液显酸性的是 、___________。
(5)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是____________ (填化学式)。此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为
。
(6)电解丙的饱和钠盐溶液的离子方程式为 。
(7)若甲的元素符号为X。已知:①X2(g)+2O2(g)===X2O4(l) ΔH=-19.5 kJ·mol-1;
②X2H4(l)+O2(g)===X2(g)+2H2O(g) ΔH=-534.2 kJ·mol-1。
则液态X2H4和液态X2O4反应生成气态X2和气态H2O的热化学方程式为
。
查看答案和解析>>
科目: 来源: 题型:
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
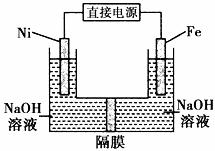 A.镍是阳极,电极反应为4OH--4e一= O2↑+ 2 H2O
A.镍是阳极,电极反应为4OH--4e一= O2↑+ 2 H2O
B.电解时电流的方向为:负极→Ni电极→溶液→Fe
电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目: 来源: 题型:
下表是在相同温度下三种酸的一些数据,下列判断正确的是
| 酸 | HX | HY | HZ | ||
| 浓度(mol/L) | 0.12 | 0.2 | 0.9 | 1 | 1 |
| 电离度 | 0.25 | 0.2 | 0.1 | 0.3 | 0.5 |
| 电离常数 | K1 | K2 | K3 | K4 | K5 |
A.在相同温度,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01
B.室温时,若在NaZ溶液中加水,则c((Z-)/ [c(HZ)• c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合液,c(X-)+c(Y-)-2c(Z-)=2c(HZ)-c(HX)-c(HY),且c(Z-)<c(Y-)<c(X-)
D.在相同温度下,K5>K4>K3
查看答案和解析>>
科目: 来源: 题型:
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结
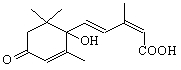 构如右图,下列关于该物质的说法正确的是
构如右图,下列关于该物质的说法正确的是
A.其分子式为C15H18O4
B.既能发生加聚反应,又能发生缩聚反应
C.分子中含有2个手性碳原子
D.既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目: 来源: 题型:
关于下列各实验装置的叙述中,不正确的是
A.图①可用于实验室制备少量Cl2或NH3
B.可用从a处加水的方法检验装置②的气密性
C.实验室也可以用装置③收集HCl气体
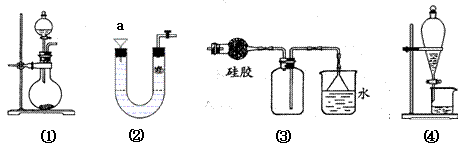 D.装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出
D.装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com