
科目: 来源: 题型:
A、B为两种短周期元素,A的原子序数大于B,且B原子的最外层电子数为A原
子最外层电子数的3倍。A、B形成的化合物是中学化学常见的化合物,该化合物熔融
时能导电。试回答下列问题:
(1)A、B的元素符号分别是________、________。
(2)用电子式表示A、B元素形成化合物的过程:_____________________________
________________________________________________________________________。
(3)A、B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了
________个阴离子;晶体中阴、阳离子数之比为__________。
(4)A、B所形成化合物的晶体的熔点比NaF晶体的熔点________,其判断的理由是
________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是( )
A.1个甘氨酸分子中存在9对共用电子
B.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构
C.H2S和CS2分子都是含极性键的极性分子
D.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
查看答案和解析>>
科目: 来源: 题型:
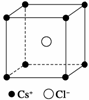
如图是CsCl晶体的晶胞结构(晶体中最小重复单元),已知晶体中两个最近的Cs+核间距离为a cm,氯化铯的式量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
A.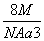 g·cm-3 B.
g·cm-3 B.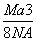 g·cm-3
g·cm-3
C.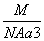 g·cm-3 D.
g·cm-3 D.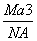 g·cm-3
g·cm-3
查看答案和解析>>
科目: 来源: 题型:
氯化铯晶胞(晶体重复的结构单位)如图甲所示,该晶体中Cs+与Cl-的个数比为1∶1,化学式为CsCl。若某晶体晶胞结构如图乙所示,其中含有A、B、C三种元素的粒子,则该晶体中A、B、C的粒子个数比为( )
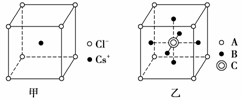
A.8∶6∶1 B.4∶3∶1
C.1∶6∶1 D.1∶3∶1
查看答案和解析>>
科目: 来源: 题型:
下列性质适合于离子晶体的是( )
A.熔点1 070℃,易溶于水,水溶液能导电
B.熔点10.31℃,液态不导电,水溶液能导电
C.能溶于CS2,熔点112.8℃,沸点444.6℃
D.熔点97.81℃,质软,导电,密度0.97 g·cm-3
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是( )
A.Na+(g)+Cl-(g)===NaCl(s) ΔH
B.Na(s)+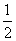 Cl2(g)===NaCl(s) ΔH1
Cl2(g)===NaCl(s) ΔH1
C.Na(s)===Na(g) ΔH2
D.Na(g)-e-===Na+(g) ΔH3
查看答案和解析>>
科目: 来源: 题型:
下面的图象是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是( )

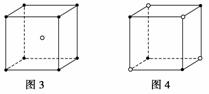
A.图1和图3 B.图2和图3
C.图1和图4 D.只有图1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com