
科目: 来源: 题型:
一种金属晶体与一种离子晶体相比较,正确的是( )
A.金属晶体一定比离子晶体微粒堆积得更密集
B.金属晶体一定比离子晶体硬度大
C.金属晶体固态时一定能导电,但离子晶体不能
D.金属晶体一定比离子晶体熔点低
查看答案和解析>>
科目: 来源: 题型:
某离子化合物DxEC6,晶胞结构如下图所示,阳离子D+位于正方体的棱的中点和正方体内部,阴离子EC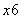 位于该正方体的顶点和面心。该化合物中x值为( )
位于该正方体的顶点和面心。该化合物中x值为( )
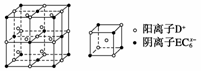
A.1 B.2 C.3 D.4
查看答案和解析>>
科目: 来源: 题型:
北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析正确的是( )
A.K3C60中既有离子键,又有极性键
B.1 mol K3C60中含有的离子数目为63×6.02×1023
C.该晶体在熔融状态下能导电
D.该物质的化学式可写为KC20
查看答案和解析>>
科目: 来源: 题型:
下列指定微粒的个数比为2∶1的是( )
A.Be2+离子中的质子和电子
B.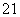 H原子中的中子和质子
H原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
查看答案和解析>>
科目: 来源: 题型:
碱金属卤化物是典型的离子晶体,它们的晶格能与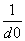 成正比(d0是晶体中最邻近的带有异性电荷离子的核间距)。下面说法错误的是( )
成正比(d0是晶体中最邻近的带有异性电荷离子的核间距)。下面说法错误的是( )
| 晶格能/kJ·mol-1 | 离子半径/pm | |
| ① | LiF LiCl LiBr LiI 1 031 845 807 752 | Li+ Na+ K+ 60 95 133 |
| ② | NaF NaCl NaBr NaI 915777 740 693 | F- Cl- Br- I- 136 181 195 216 |
| ③ | KF KCl KBr KI 812 708 676 641 |
A.晶格能的大小与离子半径成正比
B.阳离子相同、阴离子不同的离子晶体,阴离子半径越大,晶格能越小
C.阳离子不同、阴离子相同的离子晶体,阳离子半径越小,晶格能越大
D.金属卤化物晶体中,晶格能越小,还原性越强
查看答案和解析>>
科目: 来源: 题型:
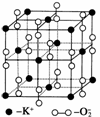
高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。右图为超氧化钾晶体的一个晶胞,则下列说法正确的是( )
A.超氧化钾的化学式为KO2,每个晶胞中含有4个K+和4个O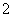
B.晶体中每个K+周围有8个O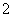 ,每个O
,每个O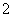 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近且相等的K+有8个
D.晶体中0价氧与-2价氧的数目之比为5∶1
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.晶体中若存在阳离子,就一定存在阴离子
B.离子晶体一定是化合物
C.离子晶体都易溶于水
D.离子晶体一定是由活泼金属和活泼非金属形成的
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.含有金属元素的晶体都是金属晶体
B.金属晶体中不一定含有金属元素
C.具有导电性的晶体一定是金属晶体
D.可以导电的物质形成的晶体不一定是金属晶体
查看答案和解析>>
科目: 来源: 题型:
下列关于金属晶体的说法中不正确的是( )
A.金属晶体中一定存在金属键
B.金属晶体中的金属键没有方向性和饱和性
C.金属晶体中金属原子只能采取最密堆积方式形成晶体
D.金属晶体中的自由电子为整个金属所共有
查看答案和解析>>
科目: 来源: 题型:
金属晶体的形成是因为晶体中存在( )
A.金属阴离子间的相互作用
B.金属原子间的相互作用
C.金属阳离子与自由电子间的相互作用
D.金属原子与自由电子间的相互作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com