
科目: 来源: 题型:
下列物质中:①金属铜 ②NaOH ③I2 ④MgCl2 ⑤Na2O2 ⑥氩气
回答下列问题:
(1)不存在化学键的是________;
(2)存在金属键的是________;
(3)只存在非极性键的是________;
(4)只存在离子键的是________;
(5)既存在离子键又存在极性键的是________;
(6)既存在离子键又存在非极性键的是________;
查看答案和解析>>
科目: 来源: 题型:
金属具有延展性的原因是( )
A.金属原子半径都较大,价电子较少
B.金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈作用
C.金属中大量自由电子受外力作用时运动速度加快
D.自由电子受外力作用时能迅速传递能量
查看答案和解析>>
科目: 来源: 题型:
下列关于金属的叙述中,不正确的是( )
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性
D.构成金属的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目: 来源: 题型:
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素原子最外层的p轨道中的电子数等于前一电子层的电子总数,X原子最外层的p轨道中有一个轨道填充了2个电子。
(1)X原子的电子排布式是______________;Y原子的价层电子轨道表示式是__。
(2)YX2的分子构型是____________,YX2的溶、沸点比ZX2________(填“高”或“低”),理由是____________________________________。
(3)YX2分子中,Y原子的杂化类型是________。YX2分子中含________个π键。
(4)下图表示一些晶体的结构(晶胞),其中代表YX2的是____________(填序号,下同),代表ZX2的是____________。
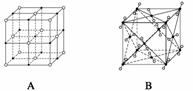
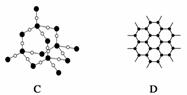
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两个成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满。
请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为______________________。
(2)B的氯化物的熔点比D的氯化物的熔点________(填“高”或“低”),理由是
________________________________________________________________________
________________________________________________________________________。
(3)F的核外电子排布式是______________________________,F的高价离子与A的简单氢化物形成的配离子的化学式为__________。
(4)A、F形成某种化合物的晶胞结构如下图所示(其中A显-3价),则其化学式为
____________。(每个球均表示1个原子)
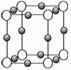
(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为____________________,其晶体中所含的化学键类型为________________,其晶体类型是____________。
查看答案和解析>>
科目: 来源: 题型:
石墨晶体具有一些独特的性质,质地较柔软但熔点很高,还具有导电性,这主要是因为石墨晶体具有一种独特的结构,石墨晶体是( )
A.原子晶体 B.金属晶体
C.分子晶体 D.混合键型晶体
查看答案和解析>>
科目: 来源: 题型:
下表是几种氯化物的熔点和沸点:
| 物质 | NaCl | MgCl2 | AlCl3 | SiCl4 |
| 熔点/℃ | 801 | 714 | 190(5×101 kPa) | -70 |
| 沸点/℃ | 1 413 | 1 412 | 180 | 57.57 |
据表中所列数据判断下列叙述与表中相吻合的是( )
A.AlCl3在加热条件下不能升华
B.SiCl4晶体属于原子晶体
C.AlCl3晶体是典型的离子晶体
D.SiCl4在晶体中有分子存在
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.金刚石晶体中的最小碳原子环由6个碳原子构成
B.Na2O2晶体中阴离子与阳离子数目之比为1∶1
C.1 mol SiO2晶体中含2 mol Si—O键
D.金刚石化学性质稳定,即使在高温下也不会和O2反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com