
科目: 来源: 题型:
标准状况下,将3.36 L CO2气体通入200 mL 1.00 mol·L-1 NaOH溶液中,充分反应后溶液中c(CO )与c(HCO
)与c(HCO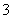 )的比值为(不考虑CO
)的比值为(不考虑CO 、HCO
、HCO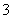 的水解)( )
的水解)( )
A.1∶1 B.1∶2
C.2∶1 D.1∶3
查看答案和解析>>
科目: 来源: 题型:
用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊 | 饱和Na2CO3溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | 澄清石灰水 |
查看答案和解析>>
科目: 来源: 题型:
二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO2所表现的化学性质或作用进行判断,其中正确的是( )
①SiO2+2NaOH===Na2SiO3+H2O
②SiO2+2C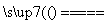 Si+2CO↑
Si+2CO↑
③SiO2+4HF===SiF4↑+2H2O
④Na2CO3+SiO2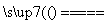 Na2SiO3+CO2↑
Na2SiO3+CO2↑
⑤SiO2+3C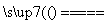 SiC+2CO↑
SiC+2CO↑
a.反应①中SiO2作为玻璃的成分被消耗,用于刻蚀玻璃
b.反应②中SiO2表现出氧化性
c.反应③中SiO2表现了酸性氧化物的通性
d.反应④符合用难挥发性的酸酐制取易挥发性酸酐的道理
e.反应⑤中SiO2未参加氧化还原反应
A.ace B.bde C.cde D.ab
查看答案和解析>>
科目: 来源: 题型:
下列关于SiO2和CO2的说法中正确的是( )
A.CO2、SiO2分别是碳酸和硅酸的酸酐
B.CO2和SiO2与水反应分别生成相应的酸
C.CO2是酸性氧化物,SiO2是两性氧化物
D.CO2和SiO2都是由相应的分子组成的
查看答案和解析>>
科目: 来源: 题型:
如何用所提供的试剂和方法除去各粉末状混合物中的杂质(括号内为杂质)。将所选答案的编号填入下表内相应的空格内(如果不需要外加试剂,则对应答案栏可空着)。
可供选择的试剂:A.盐酸 B.氢氧化钠溶液 C.氧气
D.水 E.二氧化碳
可选用的操作:①水洗 ②加热 ③高温灼烧 ④过滤
⑤结晶
| 粉末状混合物 | 选择的试剂 | 选用的操作 | |
| (1) | CaCO3(SiO2) | ||
| (2) | NaCl(SiO2) | ||
| (3) | SiO2(Fe2O3) | ||
| (4) | SiO2(CaCO3) | ||
| (5) | SiO2(NH4Cl) |
查看答案和解析>>
科目: 来源: 题型:
写出除去下列气体中混有的杂质(括号内为杂质)可采取的方法:
(1)CO(CO2):_______________________________________________。
(2)CO2(CO):_______________________________________________。
(3)CO2(O2):________________________________________________。
(4)CO2(SO2):_______________________________________________。
(5)CO2(HCl):______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究。查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐。
该小组同学利用下图装置进行实验(部分夹持仪器略)。
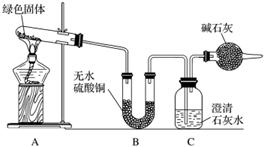
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是_______________________________________________。
(2)加热后试管中剩余的黑色物质是___________________________________________。
(3)假设该绿色物质是一种纯净物,则其化学式可能是________________________,加热分解的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(4)上述实验步骤③中的反应的离子方程式为_______________________________
________________________________________________________________________。
(5)实验装置最后的干燥管的作用是__________________________________。
(6)如果将B、C两装置对调,能否达到实验目的______(填“能”或“不能”),为什么?________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。

填写下面空白:
(1)图中标号处需加入的相应物质分别是
①____________、②____________、③____________、
④____________、⑤____________。
(2)写出①处发生反应的离子方程式________________________________________
________________________________________________________________________;
写出③处发生反应的化学方程式__________________________________________。
(3)铁红的化学式为________;分别写出铁红和氧化铜在工业上的一种主要用途:铁红________________________________________________________________________;
氧化铜________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70% Cu、25% Al、4% Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
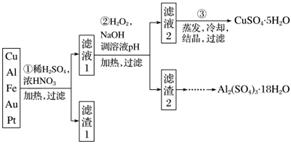
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为____________________________________________
________________________________________________________________________;
得到滤渣1的主要成分为____________。
(2)第②步加H2O2的作用是______________,使用H2O2的优点是______________;调溶液pH的目的是使______________生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是___________________________。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
甲: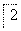
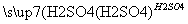
 ,蒸发、冷却、结晶、过滤
,蒸发、冷却、结晶、过滤
Al2(SO4)3·18H2O
乙: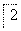
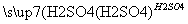

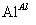

,蒸发、冷却、结晶、过滤Al2(SO4)3·18H2O
丙: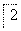
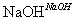

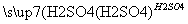

,蒸发、冷却、结晶、过滤Al2(SO4)3·18H2O
上述三种方案中,________方案不可行,原因是________________________________
________________________________________________________________________;
从原子利用率角度考虑,__________方案更合理。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com