
科目: 来源: 题型:
下列有关σ键和π键的说法错误的是( )
A.含有π键的分子在反应时,π键是化学反应的积极参与者
B.当原子形成分子时,首先形成σ键,可能形成π键
C.有些原子在与其他原子形成分子时,只能形成σ键,不能形成π键
D.在分子中,化学键可能只有π键而没有σ键
查看答案和解析>>
科目: 来源: 题型:
下列关于极性键的叙述中不正确的是( )
A.是由不同元素原子形成的共价键
B.共价化合物中必定存在极性键
C.极性键中电负性大的原子显正电性
D.共用电子对必然偏向吸引电子能力强的原子一方
查看答案和解析>>
科目: 来源: 题型:
下列有关共价键的叙述中,不正确的是( )
A.某原子跟其他原子形成共价键时,其共价键数一定等于该元素原子的价电子数
B.水分子内氧原子结合的电子数已经达到饱和,故一般不能再结合其他氢原子
C.非金属元素原子之间形成的化合物也可能是离子化合物
D.所有简单离子的核电荷数与其核外电子数一定不相等
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
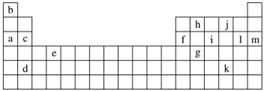
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要
的能量主要受两大因素的影响:①原子核对核外电子的吸引力,②形成稳定结构的倾向。下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | 9 550 | 11 600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:________________________________________。
②表中X可能为以上13种元素中的________(填写字母)元素,则该元素属于________区。用元素符号表示X和j所能形成的化合物的化学式是__________。
③Y是周期表中________族元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目: 来源: 题型:
不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,x越大,其原子吸引电子的能力越强。下面是某些短周期元素的x值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
(1)通过分析x值变化规律,确定Mg的x值范围:____<x(Mg)<________。
(2)推测x值与原子半径的关系是________________________________________________;
根据短周期元素的x值变化特点,体现了元素性质的________________变化规律。
(3)分别指出下列两种化合物中氧元素的化合价:HClO________,HFO________。
(4)经验规律告诉我们:成键的两原子相应元素x数值的差值为Δx,当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是________________。
(5)预测元素周期表中,x值最小的元素位于第________周期第________族(放射性元素除外)。
查看答案和解析>>
科目: 来源: 题型:
现有1~20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:
| 元素 | 物质性质或微粒结构 |
| A | M层上有2对成对电子 |
| B | B的离子与D的离子具有相同电子层结构,且可以相互组合形成干燥剂 |
| C | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)元素A的原子最外层共有________种不同运动状态的电子,有________种能量不同的电子。B的离子与D的离子相互组合形成的干燥剂的化学式是________。
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式________________________________________________________________________(用元素符号表示)。
(3)元素A与元素D相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.HD的酸性比HA酸性强
(4)C的氢化物固态时属于________晶体,该氢化物与A的最高价氧化物对应的水化物反应的化学方程式是________________________________。
查看答案和解析>>
科目: 来源: 题型:
回答下列问题:
(1)已知元素M是组成物质NH4Al(SO4)2的一种元素。元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如下表所示:
| I1 | I2 | I3 | I4 | |
| 电离能(kJ·mol-1) | 578 | 1 817 | 2 745 | 11 578 |
元素M是____________(填写元素符号)。
(2)硫原子核外有________种不同运动状态的电子,有________种不同形状的电子云。
(3)请用一个事实证明氧气的氧化性比硫的氧化性强:__________________________。
(4)写出碳原子最外层电子的电子排布图________________,该化学用语不能表达出碳原子最外层电子的________(填字母)。
a.能层 b.能级
c.所有电子云的伸展方向 d.自旋状态
查看答案和解析>>
科目: 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表数据判断,错误的是 ( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4 600 | 6 900 | 9 500 |
| Y | 580 | 1 800 | 2 700 | 11 600 |
A.元素X的常见化合价是+1价
B.元素Y是ⅡA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com