
科目: 来源: 题型:
下列物质中,属于电解质的是________,属于非电解质的是________;属于强电解质的是________,属于弱电解质的是________。
①H2SO4 ②盐酸 ③氯气 ④硫酸钡 ⑤酒精 ⑥铜
⑦冰醋酸 ⑧氯化氢 ⑨蔗糖 ⑩氨气 ⑪CO2
⑫NaHCO3
查看答案和解析>>
科目: 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)强电解质溶液的导电性比弱电解质溶液的导电性强( )
(2)BaSO4投入水中, 导电性较弱,故它是弱电解质( )
(3)弱电解质溶液中存在两种共价化合物分子( )
(4)强电解质都是离子化合物,弱电解质都是共价化合物( )
(5)CaO是强电解质,是因为它的水溶液能导电( )
(6)Cl2的水溶液能导电,所以Cl2是电解质( )
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH )________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH
)________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH )。
)。
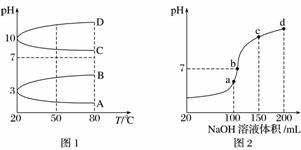
(2)如图1是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填字母)。
②室温时,0.1 mol·L-1NH4Al(SO4)2中2c(SO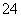 )-c(NH
)-c(NH )-3c(Al3+)=________mol·L-1(填数值)。
)-3c(Al3+)=________mol·L-1(填数值)。
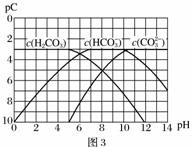
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示:
试分析图中a、b、c、d四个点,水的电离程度最大的是____________;在b点,溶液中各离子浓度由大到小的排列顺序是________________________________。
Ⅱ.pC是指极稀溶液中溶质物质的量浓度的常用对数负值,类似pH。如某溶液溶质的浓度为1×10-3mol·L-1,则该溶液中该溶质的pC=-lg10-3=3。已知H2CO3溶液中存在下列平衡:CO2+H2O??H2CO3、H2CO3??H++HCO 、HCO
、HCO ??H++CO
??H++CO
图3为H2CO3、HCO 、CO
、CO 在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:
在加入强酸或强碱溶液后,达到平衡时溶液中三种成分的pCpH图。请回答下列问题:
(1)在pH=9时,H2CO3溶液中浓度最大的含碳元素的离子为______。
(2)pH<4时,溶液中H2CO3的pC总是约等于3的原因是____________________。
(3)已知M2CO3为难溶物,则其Ksp的表达式为______;现欲将某溶液中的M+以碳酸盐(Ksp=1×10-12)的形式沉淀完全,则最后溶液中的CO 的pC最大值为______(溶液中的离子浓度小于1×10-5mol·L-1时,沉淀完全)。
的pC最大值为______(溶液中的离子浓度小于1×10-5mol·L-1时,沉淀完全)。
查看答案和解析>>
科目: 来源: 题型:
根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因
________________________________________________________________________,
其溶液中离子浓度大小顺序为____________________________________________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_____________________________________。
(3)已知纯水中存在如下平衡:H2O+H2O??H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母)。
A.向水中加入NaHSO4固体
B.向水中加Na2CO3固体
C.加热至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH溶液和⑦NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m________n(填“<”、“>”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液pH>7,用离子方程式表示原因__________________________________
________________________________________________________________________。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是________________________________________________________________________。
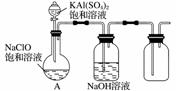
(3)某小组同学用如图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
常温下,有浓度均为1 mol·L-1的下列四种溶液:
①H2SO4溶液 ②NaHCO3溶液 ③NH4Cl溶液
④NaOH溶液
(1)这四种溶液pH由大到小的顺序是______,其中由水电离的H+浓度最小的是______。(均填序号)
(2)②中各离子浓度由大到小的顺序是____________,NaHCO3的水解平衡常数Kh=______mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时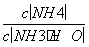 的值______(填“增大”、“减小”或“不变”)。
的值______(填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积______④的体积(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目: 来源: 题型:
某化学研究性学习小组对电解质溶液进行如下的归纳总结(均在常温下):
①pH=1的强酸溶液,加水稀释后,溶液中所有离子的浓度一定降低
②pH=2的盐酸和pH=1的盐酸,c(H+)之比为2∶1
③pH相等的四种溶液:a.CH3COONa、b.C6H5ONa、c.NaHCO3、d.NaOH,溶质的物质的量浓度由小到大的顺序为d<b<c<a
④向NH4HSO4溶液中滴加NaOH溶液至pH=7,则c(Na+)=c(SO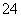 )
)
⑤已知醋酸的电离平衡常数为Ka,醋酸根离子的水解常数为Kh,水的离子积常数为Kw,则三者关系为Ka·Kh=Kw
⑥甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的2倍,则甲、乙两溶液等体积混合,混合溶液的pH可能等于7
其中归纳正确的是( )
A.全部 B.③⑤⑥
C.④⑤⑥ D.①②④
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.在Na2CO3溶液中,c(OH-)大于c(HCO )
)
B.Kw为水的离子积常数,若溶液中c2(OH-)=Kw,溶液pH可能小于7
C.1 mol·L-1 CH3COOH溶液加水稀释时,溶液中各种离子浓度均减小
D.在CH3COOH溶液中加入碱性固体物质,平衡一定向电离方向移动
查看答案和解析>>
科目: 来源: 题型:
有一种酸式盐AHB,它的水溶液呈弱碱性。则以下说法中错误的是( )
A.相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的电离程度;
B.H2B不是强酸;
C.HB-的电离程度大于HB-的水解程度;
D.该盐溶液的电离方程式一般写成:AHB??A++HB-,HB-??H++B2-
查看答案和解析>>
科目: 来源: 题型:
常温下,下列关于电解质溶液的判断正确的是( )
A.在pH=12的溶液中,K+、Cl-、HCO 、Na+可以大量共存
、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO 、SO
、SO 、K+可以大量共存
、K+可以大量共存
C.由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液中存在BOH===B++OH-
D.由0.1 mol·L-1一元酸HA溶液的pH=3,可推知NaA溶液中存在A-+H2O??HA+OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com