
科目: 来源: 题型:
依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
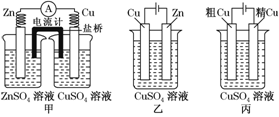
A.甲是原电池,乙是电镀装置
B.甲、乙装置中,锌极上均发生氧化反应
C.乙、丙装置中,阳极均发生氧化反应而溶解
D.乙、丙装置中,c(Cu2+)基本不变
查看答案和解析>>
科目: 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )。
A.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目: 来源: 题型:
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:________。F的原子结构示意图为________。
(2)B、D形成的化合物BD2中存在的化学键为________键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为________化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为___________________________________。
(4)A、C、D、E的原子半径由大到小的顺序是________(用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性______于F(填“强”或“弱”),并用化学方程式证明上述结论_______________________。
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。已知A与D,C与F分别同主族,D、E、F、G同周期,A分别与B、C可形成含有10个电子的共价化合物分子,B的最外层电子数是其次外层电子数的2倍,且A、B的最外层电子数之和比C的最外层电子数少1;E位于B的前一主族。
请回答下列问题。
(1)元素G在周期表中的位置为__________________,F的原子结构示意图为____________________。
(2)A、C、D三种元素组成一种常见化合物,该化合物所含的化学键类型为____________________,工业上利用某一反应可同时生产该化合物和G的单质,写出该反应的离子方程式____________________。
(3)D、E元素的最高价氧化物对应的水化物之间反应的离子方程式为___________________。
(4)含有E的简单阳离子的盐常用作净水剂,其原因为
________________________________________________________________________
(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W是原子序数依次增大的四种短周期元素。X与W可形成四面体形的共价化合物,该化合物常用作灭火剂。Y的次外层电子数等于其最外层和最内层电子数之和的2倍,Y、Z的最外层电子数之和等于W的最外层电子数。
(1)用化学符号表示X的一种核素_____________________________________________。
(2)写出Y的单质与X的最高价氧化物反应的化学方程式_________________________。
(3)Z的单质在W的单质中燃烧,生成的产物中各原子的最外层均达到8电子稳定结构的分子为________。
(4)用电子式表示Y与W形成化合物的过程为_____________。
(5)XW4的电子式为____________________________________________________。
(6)W的氢化物R是实验室一种常用试剂的主要成分,该试剂可用于实验室多种气体的制备,写出实验室制取气体时满足下列条件的离子方程式。
①R作氧化剂:__________________________________________________。
②R作还原剂:_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知X、Y是阳离子,Z是阴离子,M、N是分子,它们都由短周期元素组成,且具有以下结构特征和性质:①X、Y、M、N的核外电子总数相等;②常温下,M是极易溶于N的气体;③X与M均由相同的元素组成;④Y为单核离子,其与Z组成的物质可用于净水;⑤Z由同主族元素组成。请回答下列问题:
(1)X的电子式为______________________,Z的离子符号为______________________。
(2)X与Z形成的化合物中所含有的化学键类型为______________________。
(3)写出Y与M、N形成的混合物发生反应的离子方程式:
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________、B:________、C:________、D:________、E:________。
(2)用电子式表示离子化合物A2B的形成过程:__________________________________。
(3)写出下列物质的电子式:
①D元素形成的单质:___________________________________________________。
②E与B形成的化合物:_________________________________________________。
③A、B、E形成的化合物:_____________________________________________________。
④D与E形成的化合物:_____________________________________________。
⑤C、D、E形成的离子化合物:_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8个电子的稳定结构。则一个三硫化四磷分子中含有的共价键个数是( )
A.7个 B.9个 C.19个 D.不能确定
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、M、W为五种短周期元素,其中X、Y、Z是原子序数依次增大的同周期元素,且它们的最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是( )
A.Y、Z、W能形成含有相同电子数的简单离子,且W形成的简单离子的半径最大
B.XZ2、W2Z2均为直线形的共价化合物
C.Z与M形成的3原子化合物比Y与M形成的4原子化合物稳定
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是 ( )
A.KOH中既含有离子键也含有共价键,属于离子化合物
B.N2属于单质,不存在化学键
C.MgCl2中既含有离子键,又含有共价键
D.NH4Cl中含有共价键,又全部由非金属元素组成,属于共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com