
科目: 来源: 题型:
4,7二甲基香豆素(熔点132.6 ℃)是一种重要的香料,广泛分布于植物界中,以间甲苯酚为原料的合成反应如下:

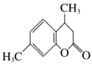 +C2H5OH+H2O
+C2H5OH+H2O
4,7二甲基香豆素
实验装置图如下:

主要实验步骤:
步骤1:向三颈烧瓶中加入60 mL浓硫酸,并冷却至0 ℃以下,边搅拌边滴入间甲苯酚30 mL(0.29 mol)和乙酰乙酸乙酯26.4 mL(0.21 mol)的混合物。
步骤2:保持在10 ℃下,搅拌12 h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗品。
步骤3:粗品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0 g。
(1)图中仪器名称:a____________,b____________。
(2)浓H2SO4需要冷却至0 ℃以下的原因是____________________________________
________________________________________________________________________。
(3)反应需要搅拌12 h,其原因是___________________________________________
________________________________________________________________________。
(4)确定最终产品是4,7二甲基香豆素的实验或方法是____________________。
(5)本次实验产率为____________。
答案 (1)恒压滴液漏斗 吸滤瓶
(2)防止浓硫酸将有机物氧化和炭化
(3)使反应物充分接触,提高反应速率
(4)测量熔点或测定其红外(紫外)光谱(及核磁共振氢谱)等 (5)89%
查看答案和解析>>
科目: 来源: 题型:
过氧化尿素是一种无毒无味的白色粉末,是一种新型的漂白剂与消毒剂。它的合成原理:CO(NH2)2+H2O2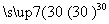 CO(NH2)2·H2O2。
CO(NH2)2·H2O2。
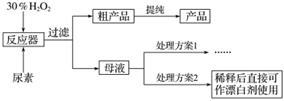
请回答下列问题:
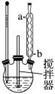
(1)流程图中反应器的装置如图所示,推测该反应的加热方式是______________________;回流管中冷水流从____________口流入;搅拌器选用的材质是玻璃而不是铁质或铝质材料的原因是__________________________。
(2)母液处理方案1可以是______________(用文字表达)。若欲从母液中分离出H2O2和尿素,可采用的操作是______(选填序号)。
A.盐析、过滤 B.减压蒸馏、结晶
C.分液、过滤 D.常压蒸馏、萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品2.000 g,溶解,在250 mL容量瓶中定容。准确量取25.00 mL于锥形瓶中,加入1 mL 6 mol·L-1的硫酸,然后用0.100 0 mol·L-1 KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液8.00 mL(KMnO4溶液与尿素不反应)。
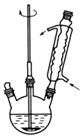
①完成并配平方程式:______MnO +______H2O2+________________________
+______H2O2+________________________
H+===______Mn2++______H2O+______。
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量________。(填“偏高”、“偏低”或“不变”)
③根据滴定结果,可确定产品中活性氧的质量分数为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知:不同温度下苯甲酸在水中的溶解度为0.18 g(4 ℃)、0.34 g(25 ℃)、6.8 g (95 ℃);乙醚的沸点为34.6 ℃。实验室常用苯甲醛制备苯甲醇和苯甲酸,其原理为
2C6H5—CHO+NaOH—→C6H5—CH2OH+C6H5—COONa
实验步骤如下:
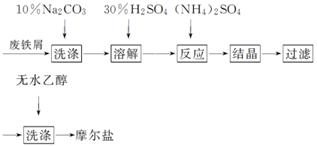
①向如图所示装置中加入适量NaOH、水和苯甲醛,混匀、加热,使反应充分进行。
②从冷凝管下口加入冷水,混匀,冷却。倒入分液漏斗,用乙醚萃取、分液。水层保留待用。将乙醚层依次用10%碳酸钠溶液、水洗涤。
③将乙醚层倒入盛有少量无水硫酸镁的干燥锥形瓶中,混匀、静置后将其转入蒸馏装置,缓慢均匀加热除去乙醚,收集198~204 ℃馏分得苯甲醇。
④将步骤②中的水层和适量浓盐酸混合均匀,析出白色固体。冷却、抽滤得粗产品,将粗产品提纯得苯甲酸。
(1)步骤②中,最后用水洗涤的作用是____________________________。将分液漏斗中两层液体分离开的实验操作方法是:先________________________,再_______________。
(2)步骤③中无水硫酸镁的作用是____________。
(3)步骤④中水层和浓盐酸混合后发生反应的化学方程式为__________________________________________;将反应后混合物冷却的目的是________________________________________________________________________。
(4)抽滤装置所包含的仪器除减压系统外,还有______、________(填仪器名称)。
查看答案和解析>>
科目: 来源: 题型:
绿矾(FeSO4·7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体,反应原理为(NH4)2SO4+FeSO4+6H2O===(NH4)2SO4·FeSO4·6H2O↓。其流程可表示为
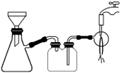
(1)洗涤中Na2CO3的主要作用是______________________________________。
(2)结晶过程中要加热蒸发溶剂,浓缩结晶。应加热到________时,停止加热。
(3)过滤是用右图所示装置进行的,这种过滤跟普通过滤相比,除了过滤速度快外,还有一个优点是________________________________________________________________________。
(4)用无水乙醇洗涤的目的是____________________________________________
________________________________________________________________________。
(5)产品中Fe2+的定量分析:制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性条件下KMnO4标准溶液滴定的方法。称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mol·L-1 KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液10.00 mL。
①本实验的指示剂是________(填字母)。
A.酚酞 B.甲基橙 C.石蕊 D.不需要
②产品中Fe2+的质量分数为______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
次硫酸氢钠甲醛(NaHSO2·HCHO·2H2O)在印染、医药以及原子能工业中应用广泛。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
步骤1:在烧瓶中(装置如图所示)加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH约为4,制得NaHSO3溶液。

步骤2:将装置A中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90 ℃下,反应约3 h,冷却至室温,抽滤。
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B的烧杯中应加入的溶液是____________。
(2)①步骤2中,反应生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是________________________________________________________________________。
②冷凝管中回流的主要物质除H2O外还有__________(填化学式)。
(3)①抽滤装置所包含的仪器除减压系统外还有______________________________________________、____________(填仪器名称)。
②滤渣的主要成分有__________、__________(填化学式)。
(4)次硫酸氢钠甲醛具有强还原性,且在120 ℃以上发生分解。步骤3中不在敞口容器中蒸发浓缩的原因是_________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
3,5二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
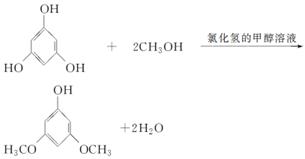
甲醇、乙醚和3,5二甲氧基苯酚的部分物理性质见下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20 ℃) /g·cm-3 | 溶解性 |
| 甲醇 | 64.7 | — | 0.791 5 | 易溶于水 |
| 乙醚 | 34.5 | — | 0.713 8 | 微溶于水 |
| 3,5二甲氧基苯酚 | — | 33~36 | — | 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是________________。②萃取用到的分液漏斗使用前需________并洗净,分液时有机层在分液漏斗的________(填“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是________;用饱和食盐水洗涤的目的是_______________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是________(填字母)。
a.蒸馏除去乙醚 b.重结晶
c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先________,再________。
查看答案和解析>>
科目: 来源: 题型:
磷酸铁(FePO4·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是_________________________________________________________。
(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:
Cr2O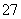 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
①在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、________和________。
②若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________mol·L-1。
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________(填序号)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4·2H2O。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为________。
查看答案和解析>>
科目: 来源: 题型:
草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)。
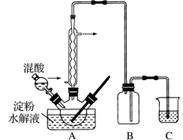
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中。
②控制反应液温度在55~60 ℃条件下,边搅拌边缓慢滴
加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2∶1.5)溶液。
③反应3 h左右,冷却,抽滤后再重结晶得草酸晶体。硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3—→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3—→6CO2↑+8NO↑+10H2O
3H2C2O4+2HNO3—→6CO2↑+2NO↑+4H2O
(1)检验淀粉是否水解完全所需用的试剂为________。
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是________________________。
(3)装置C用于尾气吸收,当尾气中n(NO2)∶n(NO)=1∶1 时,过量的NaOH溶液能将NOx全部吸收,原因是________________(用化学方程式表示)。
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是________________。
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有________。
查看答案和解析>>
科目: 来源: 题型:
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S△,Na2S2O3。常温下溶液中析出晶体为Na2S2O3·5H2O。Na2S2O3·5H2O于40~45 ℃熔化,48 ℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如图1所示。
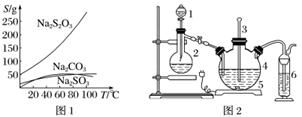
Ⅰ.现按如下方法制备Na2S2O3·5H2O:
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150 mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按图2连接好装置。
(1)仪器2的名称为________________,装置6中可放入________________(填字母)。
A.BaCl2溶液
B.浓H2SO4
C.酸性KMnO4溶液
D.NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为
①Na2CO3+SO2===Na2SO3+CO2
②Na2S+SO2+H2O===Na2SO3+H2S
③2H2S+SO2===3S↓+2H2O
④Na2SO3+S△,Na2S2O3
总反应为2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2
随着SO2气体的通入,看到溶液中有大量浅黄色固体析出,继续通SO2气体,反应约半小时至固体消失,即可停止通气和加热。若继续通入SO2,又会析出浅黄色沉淀,写出此时发生反应的离子方程式:________________________________________________。
Ⅱ.分离Na2S2O3·5H2O并测定含量:
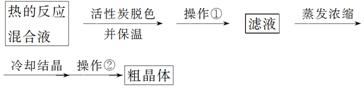
(1)为减少产品的损失,操作①为________,操作②是抽滤洗涤干燥,其中洗涤操作是用________________(填试剂)作洗涤剂。
(2)蒸发浓缩滤液直至溶液呈微黄色浑浊为止,蒸发时为什么要控制温度不宜过高________________________________________________________________________。
(3)制得的粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。KMnO4溶液应置于________(填“酸式”或“碱式”)滴定管中。
查看答案和解析>>
科目: 来源: 题型:
苯亚甲基苯乙酮俗称查尔酮,淡黄色棱状晶体,熔点58 ℃,沸点208 ℃(3.3 kPa),易溶于醚、氯仿和苯,微溶于醇。其制备原理如下:
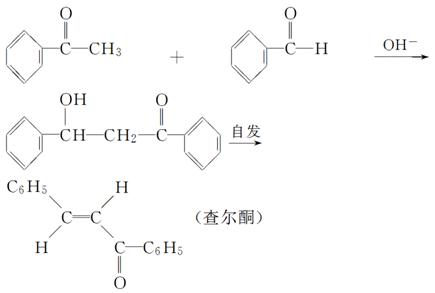
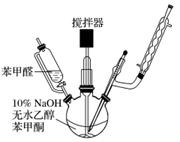
(1)制备过程中,需在搅拌下滴加苯甲醛,并控制滴加速度使反应温度维持在25~30 ℃,说明该反应是________(填“放热”或“吸热”)反应。如温度过高时,则可以采取________措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是
________________________________________________________________________。
(3)结晶完全后,需抽滤收集产物。抽滤装置所包含的仪器除减压系统外还有________、________(填仪器名称)。
(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶。加入活性炭的作用是________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com