
科目: 来源: 题型:
下表列出了周期表短周期中6种元素的有关数据:
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 原子半径(nm) | 0.075 | 0.110 | 0.152 | 0.071 | 0.186 | 0.099 |
| 最高价态 | +5 | +5 | +1 | 0 | +1 | +7 |
| 最低价态 | ﹣3 | ﹣3 | 0 | ﹣1 | 0 | ﹣1 |
根据上表信息填空:
(1)写出下列编号对应元素的元素符号:② ,③ .
(2)元素④在周期表中的位置是 .
(3)元素⑤形成的两种常见氧化物的化学式分别为 、 ,其中都含有的化学键是 .
(4)①的氢化物和⑥的氢化物反应的化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
(一)实验方法测定反应热---------中和热测定
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ |
(2)他们记录的实验数据如下:
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。
计算完成上表。△H=
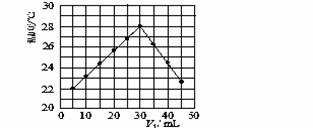
(3)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:
研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃,此反应所用NaOH溶液的浓度应为 mol/L。
(二)通过化学计算间接获得
(1)已知拆开1mol的H—H键、I—I、H—I键分别需要吸收的能量为436kJ、153kJ、299kJ。
则反应H2(g)+I2(g)=2HI(g)的反应热△H= kJ·mol-1
(2)已知:2H2(g)+ O2(g) = 2H2O (l) △H=-571.6 kJ·mol-1
H2(g)+1/2O2(g) = H2O(g) △H=-241.8 kJ·mol-1
根据上述反应确定:H2燃烧热为 kJ·mol-1;
查看答案和解析>>
科目: 来源: 题型:
以下反应中,ΔH 1 >ΔH 2 的是:
A. S(s)+O2(g) → SO2(g) ΔH1
→ SO2(g) ΔH1
S(g)+O2(g) → SO2(g) ΔH 2
→ SO2(g) ΔH 2
B. 2H2(g)+O2(g) → 2H2O(l) ΔH 1
→ 2H2O(l) ΔH 1
2H2(g)+O2(g) → 2H2O(g) ΔH 2
C. NaOH(aq)+HCl(aq)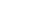 → NaCl(aq)+H2O(l) ΔH 1
→ NaCl(aq)+H2O(l) ΔH 1
NaOH(aq)+CH3COOH(aq) →CH3COONa(aq)+H2O(l) ΔH 2
D. H2(g)+F2(g)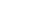 → 2HF(g) ΔH 1
→ 2HF(g) ΔH 1
H2(g)+Cl2(g)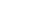 → 2HCl(g) ΔH 2
→ 2HCl(g) ΔH 2
查看答案和解析>>
科目: 来源: 题型:
.有Wn+、Xm+、Ym-、Zn-(m>n)四种离子,且W、X、Y、Z四种原子的M电子层中的电子数均为奇数。下列说法中正确的是:
A.Wn+、Xm+、Ym-、Zn-的离子半径依次增大
B.Y、Z的气态氢化物的热稳定性:HmY>HnZ
C.W、X、Y、Z的最高价氧化物对应的水化物都是强电解质
D.W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是( )
A.X的氢化物溶于水显酸性且稳定性弱于HF
B.Y的氧化物是离子化合物,Y的氢氧化物碱性比氢氧化钠弱
C.Z的氢化物的水溶液在空气中存放不易变质
D.X和Z的最高价氧化物对应的水化物都是弱酸
查看答案和解析>>
科目: 来源: 题型:
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等。它们的最高价氧化物的水化物依次为甲、乙、丙、丁。下列叙述不正确的是:

A.R的氧化物在空气中与其它物质作用可形成光化学烟雾
B.常温下丁的浓溶液可用T单质所制的容器来盛装
C.丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体
D.甲、乙、丙、丁受热均易分解
查看答案和解析>>
科目: 来源: 题型:
下列有关热化学方程式的书写及对应的表述均正确的是:
A.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量。则Fe(s)+S(s)===FeS(s) ΔH=-95.6 kJ·mol-1
B.稀醋酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
C.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
D.已知2C(s)+O2(g)=2CO(g)ΔH=-221 kJ·mol-1,则C的燃烧热ΔH=-110.5 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是:

A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中一定只有共价键
C.W、X、Z三种元素最高价氧化物对应水化物的酸性逐渐减弱
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目: 来源: 题型:
下列叙述错误的是:
①热稳定性:H2O>HF>H2S ②熔点:Al>Na>K
③ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥已知H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H= -114.6kJ·mol-1 则中和热为57.3kJ·mol-1
⑦两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键
A.②④⑥ B.①⑤⑥ C.②③④ D.①⑤⑦
查看答案和解析>>
科目: 来源: 题型:
天然存在的金属钫(Fr)极微量。它的21种已知同位素都有放射性。它是碱金属元素中最重的元素。根据它在周期表中的位置预言其性质,其中不正确的是:
A.在空气中燃烧时生成氧化物Fr2O B.在碱金属元素中具有最大的原子半径
C.氧化物对应的水化物是极强的碱 D.其单质的熔点比金属钠的熔点低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com