
科目: 来源: 题型:
下列说法中不正确的是( )
A.一般σ键比π键电子云重叠程度大,形成的共价键强
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键
D.N2分子中有一个σ键,两个π键
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.同一原子中,2p、3p、4p能级的轨道数依次增多
B.电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则
C.共价键都有方向性
D.正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族
查看答案和解析>>
科目: 来源: 题型:
取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算:
(1)原混合液中Na2SO4的物质的量浓度为_________ mol ·L-1。
(2)产生的气体在标准状况下的体积为___________ L。
(3)过滤出沉淀后,计算所得滤液的物质的量浓度(设反应后溶液的体积为200mL)。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组设计实验,用于制取SO2并探究SO2的某些性质。制取
SO2反应的化学方程式为:Na2SO3+2H2SO4=Na2SO4+SO2↑+H2O,产生的气体通入下图所示装置:
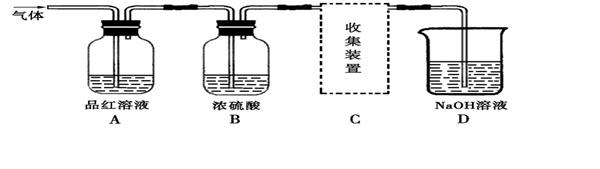
【实验探究】
(1)将12.6g的Na2SO3与足量的浓硫酸反应可制得SO2的体积为___________L(标准状况,Na2SO3的摩尔质量为126g·mol-1),该制取SO2的反应___________(填“是”或“不是”)氧化还原反应。
(2)A装置观察到的现象是______________,说明SO2具有___________(填“漂白性”或“还原性”)。
(3)B装置中浓硫酸的作用是___________(填“干燥剂”或“氧化剂”)。
(4)D装置的作用是______________________
【实验讨论】
对上图中的C处,甲乙两同学都选用右图装置,但对连接方式持有不同意见。
 甲同学认为:SO2气体应从a处通入集气瓶中。
甲同学认为:SO2气体应从a处通入集气瓶中。
乙同学认为:SO2气体应从b处通入集气瓶中。
你认为___________(填“甲”或“乙”)同学的看法是正确的。
(已知:同等条件下二氧化硫的密度大于空气)
【联系实际】
SO2对环境的影响较大,为了减少SO2对空气的污染,请你提出一种有效的措施________________________ ________________。
查看答案和解析>>
科目: 来源: 题型:
针对下面10种元素,完成以下各小题。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是___________(填名称)。
(2)化学性质最不活泼的元素是___________(填元素符号)。
(3)Al的原子结构示意图为___________________。
(4)C与N相比,原子半径较小的是___________。
(5)最高价氧化物对应的水化物碱性最强的是___________(填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________。
(7)S和Cl相比,元素非金属性较强的是___________。
(8)可用来制造光导纤维的物质是___________,晶体硅的主要用途是___________(写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:____________________________________________________
查看答案和解析>>
科目: 来源: 题型:
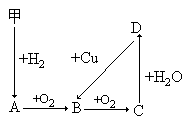 单质甲能发生如下变化(反应条件均未标明),其中A、B、C、D中都含有相同的一种元素,试举出两组符合题意的实例,写出对应各物质的分子式
单质甲能发生如下变化(反应条件均未标明),其中A、B、C、D中都含有相同的一种元素,试举出两组符合题意的实例,写出对应各物质的分子式
甲_____A._____B._____C._____D._____
甲_____A._____B._____C._____D._____
查看答案和解析>>
科目: 来源: 题型:
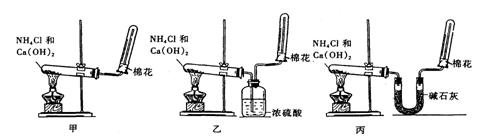 为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置
为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置
(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) 。
(2)写出制取氨气的化学方程式 。
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。
根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 ,乙物质的化学式是 •
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
。
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
查看答案和解析>>
科目: 来源: 题型:
将10 mL NO和NO2的混合气体通入装满水的倒立在水槽中的量筒里,充分反应后,最后剩余6mL气体,则原混合气体中NO的体积为
A、1mL B、4mL C、5mL D、7mL
查看答案和解析>>
科目: 来源: 题型:
把含硫酸铵和硝酸铵的混合液2a L分成两等份。一份加入bmol NaOH并加热,恰好把NH3全部赶出;另一份需消耗cmol BaCl2沉淀反应恰好完全,则原溶液中NO3- 的浓度为 ( )
A 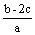 B
B 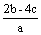 C
C 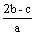 D
D 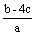
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com