
科目: 来源: 题型:
下列性质的递变中,正确的是( )
A.O、Na、S的原子半径依次增大 B.LiOH、KOH、CsOH的碱性依次增强
C.HF、NH3、SiH4的稳定性依次增强 D.HCl、HBr、HI的还原性依次减弱
查看答案和解析>>
科目: 来源: 题型:
将纯锌片和纯铜片按右图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的酸性均减弱 D.产生气泡的速率甲比乙慢
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏伽德罗常数的值。下列叙述正确的是( )
A.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
B.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA
C.0.1mol·L-1的NH4NO3溶液中氮原子数为0.2NA
D.标准状况下, 22.4L苯中C—H键数为6NA
查看答案和解析>>
科目: 来源: 题型:
航天飞机用铝粉和高氯酸铵(NH4ClO4)的混合物作为固体燃料,点燃时铝粉氧化并放出大量热量引发高氯酸铵分解:NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O。下列对此反应叙述不正确的是( )
A.上述反应属于分解反应
B.上述反应瞬间产生大量高温气体推动航天飞机飞行
C.上述反应从能量变化上说,主要是化学能转化为热能和动能
D.该反应中高氯酸铵只起氧化剂作用
查看答案和解析>>
科目: 来源: 题型:
下列化学用语书写正确的是( )
A.氯离子的结构示意图: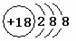 B.作为相对原子质量测定标准的碳核素:
B.作为相对原子质量测定标准的碳核素: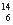 C
C
C.氯化镁的电子式: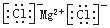
D.用电子式表示氯化氢分子的形成过程:
查看答案和解析>>
科目: 来源: 题型:
元素周期表是一座开放的“元素大厦”,元素大厦尚未充满。若发现119号元素,请您在元素大厦中安排好它的“房间” ( )
A.第七周期第0族 B.第六周期ⅡA族 C.第八周期第ⅠA族 D.第七周期第ⅦA族
查看答案和解析>>
科目: 来源: 题型:
现有浓度均为0.1 mol·L-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_____________________ _____________________________________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是__________________________________________________。
(3)已知T ℃,KW=1×10-13,则T ℃________25 ℃(填“>”、“<”或“=”)。在T ℃时将pH=11的NaOH溶液a L与pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=________。
(4)25 ℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=________(填数据);
②若x+y=13,则a/b=________(填数据);
③若x+y>14,则a/b=________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为________(填表达式)。
查看答案和解析>>
科目: 来源: 题型:
某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20 mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2 cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________________;
(2)上述B步骤操作的目的是________________________________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是___________________________________________________________;
(4)判断到达滴定终点的实验现象是_______________________________;
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是__________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知:常温下,A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为________。
a.大于7 b.等于7 c.小于7
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为________mol/L,B溶液中水电离出的氢离子浓度为________mol/L。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com