
科目: 来源: 题型:
下列做法会对人体健康造成较大危害的是 ( )
A.用小苏打(NaHCO3)发酵面团制作馒头
B.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
C.用SO2漂白银耳、腐竹等食品
D.自来水中通入少量Cl2进行杀菌消毒
查看答案和解析>>
科目: 来源: 题型:
世界气候大会与2009年在丹麦首都哥本哈根召开,商讨2012年至2020年全球温室气体减排协议。下列物质属于温室气体的是( )
A.可吸入颗粒 B.氮气 C.氧气 D.二氧化碳
查看答案和解析>>
科目: 来源: 题型:
下列观点不正确的是 ( )
A.化学是一门以实验为基础的科学
B.从宏观看,物质有时处在相对静止状态,但从微观看,则是永恒运动的
C.运用分类的方法,可根据物质所属的类别预测物质的性质
D.世界是由物质构成的,物质都是由分子和原子构成
查看答案和解析>>
科目: 来源: 题型:
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表)。设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
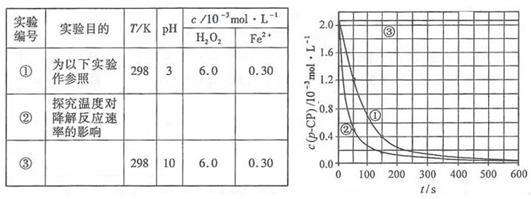 实验测得p-CP的浓度随时间变化的关系如右上图。
实验测得p-CP的浓度随时间变化的关系如右上图。
(2)请根据右上图实验①曲线,计算降解反应在50~150 s内的反应速率
v(p-CP) =__________mol·L-1·s-1。
(3)实验①②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因: _______________________________________________________________________。
(4)实验③得出的结论是:pH等于10时,_______________________。
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来,根据上图中信息,给出一种迅速停止反应的方法_____________________________。
查看答案和解析>>
科目: 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。
(3)830℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡 移动(选填“向正反应方向”、“向逆反应方向”、“不”)。
(4)若 830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,其化学平衡常数K 1.0(选填“大于”、“小于”、“等于”)
(5)若1200℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、
2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为 。(选填“正反应方向”、“逆反应方向”、“不移动”)
查看答案和解析>>
科目: 来源: 题型:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000 mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2 mL。
 试回答下列问题:
试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)该小组在步骤①中的错误是 ,
由此造成的测定结果 (偏高、偏低或无影响)。
(3)右图,是某次滴定时的滴定管中的液面,其读数为 mL。
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
请计算待测烧碱溶液的浓度为 mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
1)稀强酸、稀强碱反应生成1mol水时放出57.3 kJ的热。
① 实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式 ;
② 分别取100 mL 0.50 mol/L盐酸与100 mL 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容c = 4.18 J/(g·℃)。实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃。
则实验测得的中和热△H=____ ___(保留1位小数)
③ 如果用含1 mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”);理由是____________
(2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO。理论上每消耗标况下22.4 L NO就能放出290 kJ的热。写出该反应的热化学方程式
查看答案和解析>>
科目: 来源: 题型:
2 SO2(g) + O2(g) 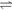 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的 H=-99 kJ·mol-1。
H=-99 kJ·mol-1。
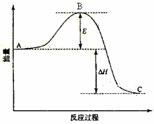
请回答下列问题:
(1)图中A、C分别表示______________、______________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____,理由是______________________________________;
(2)图中ΔH=___________kJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式__________________________________________________________________;
(4)如果反应速率v(SO2)为0.05 mol·L-1·min-1,则v(O2)=__________mol·L-1·min-1、v(SO3)=___________ mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH(要求计算过程)________________________。
查看答案和解析>>
科目: 来源: 题型:
如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是( )
A.石墨和金刚石的转化是物理变化
B.C(s、石墨)== C(s、金刚石)
△H= +1.9 kJ•mol-1
C.金刚石的稳定性强于石墨
D.1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目: 来源: 题型:
一定条件下,合成氨气反应达到平衡时,测得混合气体中氨气的体积分数为20.0% ,与反应前的体积相比,反应后体积缩小的百分率是
A.16.7% B.20.0% C.80.0% D.83.3%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com