
科目: 来源: 题型:
在密闭容器中进行下列反应:X2(g)+Y2(g)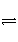
 2Z(g)。已知X2、Y2和Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.2 mol·L-1,当反应在一定条件下达到平衡时,各物质的浓度有可能是( )
2Z(g)。已知X2、Y2和Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.2 mol·L-1,当反应在一定条件下达到平衡时,各物质的浓度有可能是( )
A.Z为0.3 mol·L-1 B.Y2为0.4 mol·L-1
C.X2为0.2 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
反应CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的是( )
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
查看答案和解析>>
科目: 来源: 题型:
已知反应mX(g)+nY(g)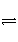
 qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g)的ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)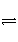
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目: 来源: 题型:
往平底烧瓶中放入氢氧化钡晶体[Ba(OH)2·8H2O]和固态氯化铵晶体,塞紧瓶塞。在瓶底和木板间滴少量水,如下图所示。一会儿,就会发现瓶内固态物质变稀并有液体产生,瓶壁变冷,小木板上因少量水冻结而被烧瓶黏住,这时打开瓶塞,出来的气体有氨味。这是自发地发生了反应:Ba(OH)2·8H2O(s)+2NH4Cl(s)===BaCl2(s)+2NH3(g)+10H2O(l)
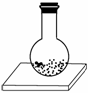
下列结论正确的是( )
A.自发反应一定是放热反应
B.自发反应一定是吸热反应
C.有的吸热反应也能自发进行
D.吸热反应不能自发进行
查看答案和解析>>
科目: 来源: 题型:
硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3)等,其中硫酸最为重要,在工业上有广泛的应用。
完成下列计算:
(1) 浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况),若将反应后的溶液稀释至500mL,该溶液中硫酸铜的物质的量浓度为 mol·L-1;
(2)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度为 mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
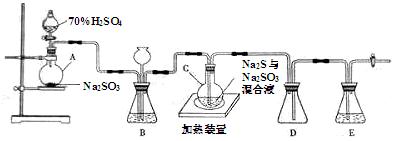
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)装置A中反应的化学方程式为 。
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (I)
2H2S+SO2=3S+2H2O (II)
S+Na2SO3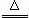 Na2S2O3 (III)
Na2S2O3 (III)
为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
查看答案和解析>>
科目: 来源: 题型:
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差4,戊的单质是空气中含量最多的成分,,丁与辛属同周期元素,
 (1)用元素符号表示甲、乙、丁的金属性从强到弱的顺序 ;
(1)用元素符号表示甲、乙、丁的金属性从强到弱的顺序 ;
(2)用元素符号表示辛、己、戊的原子半径从大到小的顺序 ;
(3)丙与庚的原子核外电子数相差 ;
(4)戊单质电子式为 ,写出一种含戊、己两种元素的离子化合物的化学式 。
查看答案和解析>>
科目: 来源: 题型:
焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式 ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平) MnO4-+ C+ H2O—— MnO2+ ① +CO32-,则 ① 处应该填入的微粒化学式为 ;
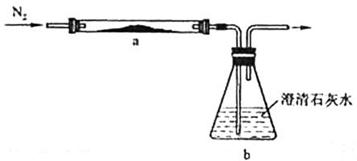 (3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
写出反应管a中发生的所有反应的化学方程式
查看答案和解析>>
科目: 来源: 题型:
短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A的原子结构示意图是___________ E的电子式为___________;
(2)D在周期表中的位置是 ______。它的下一周期同族元素最高价氧化物对应的水化物的分子式为___________;
(3)C与水反应的化学方程式是_________________________________,写出所得溶液中含有10个电子的微粒符号___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com