
科目: 来源: 题型:
常温下,对于 ① 0.1 mol/L CH3COOH溶液 ② pH = 1 HCl溶液 ③ pH =13的NaOH溶液④ 0.1 mol/L CH3COONa溶液,下列说法正确的是( )
A.①和②分别稀释100倍后的pH: ①> ②
B.水电离出的c(OH-):④>③> ① > ②
C.①和③混合后溶液呈中性:c(Na+) /c(CH3COO-) < 1
D.①和④混合后溶液呈酸性:c(Na+) / c(CH3COO-)>1
查看答案和解析>>
科目: 来源: 题型:
现有5种短周期元素X、Y、Z、Q、W,原子序数依次增大,在周期表中X原子的半径最小;X和W同主族;Y原子的核外电子总数是其次外层电子数的3倍,Q是地壳中含量最高的元素。下列说法不正确的是( )
A.原子半径:Y<Q<W
B.ZX3可使紫色石蕊试液变蓝
C.X、Z、Q可组成离子化合物或共价化合物
D.X2Q2、Y2X6两种分子中含有的电子数、化学键种类都相同
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列说法正确的是( )
A.0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA
B.标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于NA
C.铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标准状况下)
D.标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA
查看答案和解析>>
科目: 来源: 题型:
化学与生产,生活密切相关,下列有关说法中正确的是( )
A.玻璃、水泥、水晶都是硅酸盐制品
B.蚕丝和棉花的组成元素相同,结构不同,因而性质不同
C.石油的分馏和煤的气化、液化,涉及的都是物理变化
D.纤维素不能被人体消化吸收,但能促进肠道的蠕动,对人体有益
查看答案和解析>>
科目: 来源: 题型:
一定温度下,分别往容积均为5 L的甲(恒压密闭容器)、乙(恒容密闭容器)中各加入0.5 mol无色的N2O4气体,立即出现红棕色。当反应进行到2 s时,测得乙容器中N2O4的浓度为0.09 mol·L-1。经过60 s乙容器中的反应达到平衡(反应过程中两个容器的温度均保持恒定)。

(1)容器中气体出现红棕色的原因是(用化学方程式表示)
________________________________________________________________________。
(2)前2 s内,乙容器中以N2O4的浓度变化表示的平均反应速率为____________________。
(3)达到平衡时,甲容器中反应所需的时间______60 s(填“大于”、“小于”或“等于”,下同);两容器中都达到平衡时,N2O4的浓度:甲__________乙,反应过程中吸收的能量:甲__________乙。
(4)两容器都达到平衡后,若要使甲、乙中N2O4浓度相等,不能采取的措施是__________。
A.保持温度不变,适当压缩甲容器
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量N2O4
D.保持容器体积不变,使甲容器降温
查看答案和解析>>
科目: 来源: 题型:
以化学平衡移动原理为依据,解释以下事实。
(1)在氨水中加入氢氧化钠溶液,有氨气逸出
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)合成氨工业中将氨气液化,可以提高氨的产量
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)用热水溶解碳酸钠晶体(Na2CO3·10H2O),可提高去污能力
________________________________________________________________________
________________________________________________________________________。
(4)打开冰冻啤酒倒入玻璃杯,杯中立即泛起大量泡沫
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在密闭容器中进行下列反应CO2(g)+C(s)2CO(g) ΔH>0,达到平衡后,改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加C的用量,平衡__________,c(CO)________。
(2)减小密闭容器的体积,保持温度不变,则平衡____________,c(CO2)________。
(3)通入N2,保持密闭容器的体积和温度不变,则平衡____________,c(CO2)________。
(4)保持密闭容器的体积不变,升高温度,则平衡____________,c(CO2)________。
查看答案和解析>>
科目: 来源: 题型:
对于反应2SO2+O2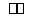 2SO3,下列判断正确的是(双选)( )
2SO3,下列判断正确的是(双选)( )
A.2体积SO2和足量O2反应,必定生成2体积SO3
B.其他条件不变,增大压强,平衡必定向右移动
C.平衡时,SO2消耗速率必定等于O2生成速率的2倍
D.平衡时,SO2浓度必定等于O2浓度的2倍
查看答案和解析>>
科目: 来源: 题型:
对已达化学平衡的反应:2X(g)+Y(g)  2Z(g),减小压强时,对反应产生的影响是( )
2Z(g),减小压强时,对反应产生的影响是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com