
科目: 来源: 题型:
下列事实能用键能大小来解释的是( )
①N2的化学性质比O2稳定 ②金刚石的熔点高于晶体硅 ③惰性气体一般难发生化学反应 ④通常情况下,溴呈液态,碘呈固态
A.①② B.①③
C.②④ D.③④
查看答案和解析>>
科目: 来源: 题型:
关于共价键的说法,正确的是( )
A.一般来说σ键键能小于π键键能
B.原子形成共价键的数目等于基态原子的未成对电子数
C.相同原子间的双键键能是单键键能的两倍
D.所有不同原子间的键至少具有弱极性
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.分子的结构是由键长决定的
B.共价键的键能越大,共价键越牢固,含有该键的分子越稳定
C.CF4、CCl4、CBr4、CI4中C—X键的键长、键角均相等
D.H2O分子中2个O—H键夹角为180°
查看答案和解析>>
科目: 来源: 题型:
N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为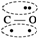 ,其中椭圆框表示π键,下列说法不正确的是( )
,其中椭圆框表示π键,下列说法不正确的是( )
A.N2分子与CO分子中都含有叁键
B.N2分子与CO分子中的π键并不完全相同
C.N2分子与CO分子中的价电子总数相等
D.N2分子与CO分子的化学性质相同
查看答案和解析>>
科目: 来源: 题型:
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(1)根据表中数据,在该题图中相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
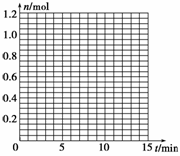
(2)体系中发生反应的化学方程式是____________;
(3)列式计算该反应在0~3 min时间内产物Z的平均反应速率:__________________;
(1) 该反应达到平衡时反应物X的转化率α等于___________________________;
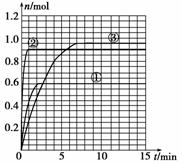
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如上图所示),则曲线①、②、③改变的实验条件分别是:
①________;②________;③________。
查看答案和解析>>
科目: 来源: 题型:
某化学反应2A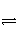
 B+D在四种不同条件下进行。B、D起始浓度为0,反应物A
B+D在四种不同条件下进行。B、D起始浓度为0,反应物A
的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20 min时间内的平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=______mol·L-1,反应经20 min就达到了平衡,可推测实验2中还隐含的条件是____________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______v1(填“>”、“=”或“<”),且c3______1.0 mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应的正反应是______反应(填“吸热”或“放热”),理由是________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)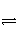
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______________________________________。
(2)该反应为________(填“吸热”或“放热”)反应。
(3)能判断该反应是否达到化学平衡状态的依据是________(填字母序号)。
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为______℃。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com