
科目: 来源: 题型:
某学校设计了一节实验活动课,让学生从废旧电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个实验过程如下。回答有关问题。
(1)干电池的基本构造和工作原理
如图为干电池的基本构造图。干电池工作时负极上的电极反应是
__________________________,MnO2的作用是除去正极上的产物H2,该反应方程式为2MnO2+H2===Mn2O3+H2O。
(2)锌皮和碳棒的回收
用钳子和剪子剪开待回收的干电池的锌筒,将锌皮和碳棒取出,并用毛刷刷干净,将电池内的黑色粉末移入烧杯中。
(3)氯化铵、氯化锌的提取、检验和分离
①如何从黑色粉末中提取NH4Cl和ZnCl2等晶体的混合物?写出简要的实验步骤________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
②设计简单的实验证明所得晶体中含有NH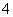 。
。
实验步骤
________________________________________________________________________
________________________________________________________________________;
实验现象
________________________________________________________________________;
有关的离子方程式
________________________________________________________________________。
③用________的方法可将NH4Cl和ZnCl2的晶体混合物分离开。
④最后剩余的黑色残渣的主要成分是MnO2,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中要用到的主要仪器有
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
烧过菜的铁锅未及时洗涤(残液中含NaCl等),第二天便出现红棕色锈斑。下列反应表示整个过程可能发生的变化,其中不符合事实的是( )
A.2H2O+O2+4e-===4OH-
B.Fe-3e-===Fe3+
C.Fe2++2OH-===Fe(OH)2↓
D.4Fe(OH)2+O2+2H2O===4Fe(OH)3
查看答案和解析>>
科目: 来源: 题型:
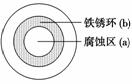 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )
A.液滴中的Cl- 由a区向b区迁移
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-===4OH-
C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2 ,进一步氧化、脱水形成铁锈
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-===Cu2+
查看答案和解析>>
科目: 来源: 题型:
据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为:2Zn+O2===2ZnO,原料为锌粒、电解液和空气。则下列叙述正确的是(双选)( )
A.锌为正极,空气进入负极反应
B.负极反应为Zn-2e-===Zn2+
C.正极发生氧化反应
D.电解液肯定不是强酸
查看答案和解析>>
科目: 来源: 题型:
锌锰干电池在放电时,电池总反应方程式可以表示为Zn+2MnO2+2NH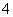 ===Zn2++Mn2O3+2NH3+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
===Zn2++Mn2O3+2NH3+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
A.MnO2和NH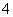 B.Zn2+和NH
B.Zn2+和NH
C.Zn D.碳棒
查看答案和解析>>
科目: 来源: 题型:
取3.4 g只含羟基、不含其它官能团的液态饱和多元醇,置于5.00 L氧气中,经点燃,醇完全燃烧。反应后气体体积减少了0.56 L。将气体经CaO吸收,体积又减少2.80 L(所取体积均在标准状况下测定)。
(1)求出该醇中C、H、O的原子数之比。
(2)由以上比值能否确定该醇的分子式,为什么?
(3)如果将该多元醇的任意一个羟基换成一个卤原子,所得到的卤代物都只有一种,试写出该饱和多元醇的结构简式。
查看答案和解析>>
科目: 来源: 题型:
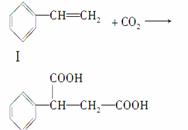
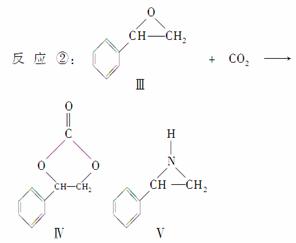
)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。CO2与化合物Ⅰ反应生成化合物Ⅱ,与化合物Ⅲ反应生成化合物Ⅳ,如反应①和②所示(其他试剂、产物及反应条件均省略)。
反应①:
Ⅱ
(1)化合物Ⅰ的分子式为________,1 mol该物质完全燃烧需消耗________mol O2。
(2)由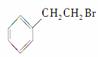 通过消去反应制备Ⅰ的化学方程式为
通过消去反应制备Ⅰ的化学方程式为
________________________________________________________________________
________________________________________________________________________(注明反应条件)。
(3)Ⅱ与过量C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为
________________________________________________________________________。
(4)在一定条件下,化合物Ⅴ能与CO2发生类似反应②的反应,生成两种化合物(互为同分异构体),请写出其中任意一种化合物的结构简式: __________________________
________________________________________________________________________。
(5)与CO2类似,CO也能被固定和利用。在一定条件下,CO、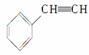 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,下列关于Ⅵ和Ⅶ的说法正确的有________________(双选,选字母)。
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应,下列关于Ⅵ和Ⅶ的说法正确的有________________(双选,选字母)。
A.都属于芳香烃衍生物
B.都能使溴的四氯化碳溶液褪色
C.都能与Na反应放出H2
D.1 mol Ⅵ或Ⅶ最多能与4 mol H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回到烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入________,目的是
________________________________________________________________________。
(2)反应中加入过量的乙醇,目的是
________________________________________________________________________
________________________________________________________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加醋酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是__________________
________________________________________________________________________。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。

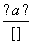
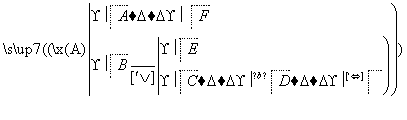
试剂a是____________,试剂b是________;分离方法①是________,分离方法②是________,分离方法③是________________。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是____________。
查看答案和解析>>
科目: 来源: 题型:
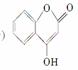 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
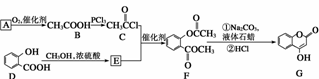
(1)A与银氨溶液反应有银镜生成,则A的结构简式是
________________________________________________________________________。
(2)B→C的反应类型是______________。
(3)E的结构简式是
________________________________________________________________________。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
________________________________________________________________________
_______________________________________________________________________。
(5)下列关于G的说法正确的是________。
a.能与溴单质反应
b.能与金属钠反应
c.1 mol G最多能和3 mol氢气反应
d.分子式是C9H6O3
查看答案和解析>>
科目: 来源: 题型:
300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式为:

(1)用没食子酸制造墨水主要利用了________类化合物的性质(填代号)。
A.醇 B.酚 C.油脂 D.羧酸
(2)没食子酸丙酯具有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为______________。
(3)尼泊金酯是对羟基苯甲酸与醇形成的酯类化合物,是国家允许使用的食品防腐剂。尼泊金丁酯的分子式为__________________,其苯环只与-OH和-COOR两类取代基直接相连的同分异构体有______种。
(4)写出尼泊金乙酯与氢氧化钠溶液加热反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com