
科目: 来源: 题型:
)(1)用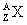 表示原子:
表示原子:
①中性原子的中子数:N= 。
②阳离子的中子数:AXn+共有x个电子,则N= (用A、x、n表示)。
③阴离子的中子数:AXn-共有x个电子,则N= (用A、x、n表示)。
④分子或原子团的中子数:12C16O2分子中,N=_______。
(2)已知某元素R原子的质量数为A,其阴离子Rn-含有x个电子,则mg Rn-中含中子的物质的量是 mol。
查看答案和解析>>
科目: 来源: 题型:
氯的原子序数为17,37Cl和35Cl是氯的两种同位素,下列说法正确的是 ( )
A.35Cl所含质子数为18
B. mol的H35Cl分子所含中子数约为6.02×1023
mol的H35Cl分子所含中子数约为6.02×1023
C.3.5 g的35Cl2气体的体积为2.24 L
D.35Cl2气体的摩尔质量为70 g·mol-1
查看答案和解析>>
科目: 来源: 题型:
最近医学界通过用放射性14C来标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA来杀死细胞,从而抑制艾滋病(AIDS),则有关14C的叙述正确的是 ( )
A.与C60中普通碳原子的化学性质不同
B.与14N中含的中子数相同
C.是C60的同素异形体
D.与12C互为同位素
查看答案和解析>>
科目: 来源: 题型:
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是 ( )
A.Th元素的质量数是232
B.Th元素的相对原子质量是231
C.232Th转化成233U是化学变化
D.230Th和232Th的化学性质相同
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是 ( )
A.核素就是同位素
B.元素的金属性强弱与元素失去电子数的多少成正比
C.具有相同质子数的微粒一定是同一种元素
D.核内中子数为N的R2+,质量数为A,则该离子的核外电子数为A-N-2
查看答案和解析>>
科目: 来源: 题型:
美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为 ( )
A.47 B.175 C.61 D.57
查看答案和解析>>
科目: 来源: 题型:
重水(D2O)是重要的核工业原料,下列说法错误的是 ( )
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1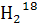 O与
O与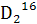 O的相对分子质量相同
O的相对分子质量相同
查看答案和解析>>
科目: 来源: 题型:
为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
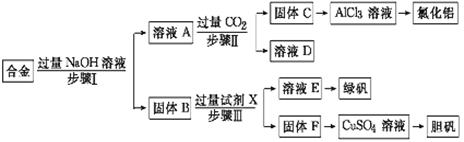
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
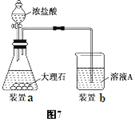
(3)进行步骤Ⅱ时,该小组用如图7所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
查看答案和解析>>
科目: 来源: 题型:
常见元素A、B、M组成的四种物质发生反应:甲+乙 丙+丁,其中甲由A和M组成,乙由B和M组成,丙只含M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则甲的电子式为 ;生成标准状况下5.6L丙转移移电子数为 ;常温下丁溶液pH 7,用离子方程式解释 。
(2)若丁为能使品红褪色的无色气体,丙为常见紫红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。则:
①A在周期表中位置为
②将丁通至FeCl3溶液中的现象为
离子反应方程式为
③正确书写上述生成丙的化学方程式
④向MCl2的溶液中通入丁,可观察到白色的MC1沉淀,写出该反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com