
科目: 来源: 题型:
正确掌握化学用语是学好化学的基础,下列有关表述正确的是
( )。
A.H、D、T互为同素异形体
B.氨分子中的化学键为非极性共价键
C.NH4Cl的电子式:
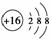
D.S2-的结构示意图:
查看答案和解析>>
科目: 来源: 题型:
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素大厦”中安排好它的“房间”
( )。
A.第七周期0族 B.第六周期第ⅡA族
C.第八周期第ⅠA族 D.第七周期第ⅦA族
查看答案和解析>>
科目: 来源: 题型:
现用98%的浓H2SO4(ρ=1.84 g·cm-3)配制浓度为0.5 mol·L-1的稀硫酸500 mL。
(1)选用的玻璃仪器除烧杯、玻璃棒外,还需__________________________。
(2)请将下列操作按正确的顺序把序号填写在横线上
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加水至刻度线
D.洗涤所用仪器
E.稀释浓H2SO4
F.将溶液转入容量瓶
其操作的正确顺序为_____________________________________________________。
(3)简要回答下列问题:
①所需浓H2SO4的体积为______ mL。
②如果实验室有15 mL、20 mL、25mL的量筒,选用______ mL的量筒最好。量取时发现量筒不干净,用水洗净后直接量取将使实验最终结果______(填“偏高”、“偏低”或“无影响”)。
③在转入容量瓶前烧杯中液体应________________,否则会使浓度________(填“偏高”、“偏低”或“无影响”)。
④定容时必须使溶液凹液面最低处与刻度线相切,若俯视会使结果________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
一学生设计了如下实验方案分离NaCl和CaCl2两种固体的混合物:





回答下列问题:
(1)B物质的名称是________;
(2)此实验分离得到的NaCl,经分析含有杂质,是因为上述方法中其中一步设计有错误,请写出改正的方法:__________________________________。
(3)加入足量Na2CO3溶液后的操作名称是________,所需使用的玻璃仪器是_______。
查看答案和解析>>
科目: 来源: 题型:
用AgNO3溶液和NaCl、MgCl2、AlCl3三种溶液分别反应时,(1)若把同体积、同物质的量浓度的三种溶液中的Cl-全部沉淀下来,所需AgNO3溶液的体积比是________;
(2)若把同体积的三种溶液中的Cl-全部沉淀下来,所用AgNO3溶液体积相同,则此三种溶液中溶质的物质的量浓度之比为______________,生成沉淀的质量比为______________。
查看答案和解析>>
科目: 来源: 题型:
实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)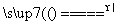 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)写出该反应的离子方程式:_____________________________________________。
(2)在反应中MnO2发生________(填“氧化”或“还原”,下同)反应,Cl2是__________产物。
(3)当0.1 mol MnO2参加反应时,转移的电子数为______,被氧化的HCl为________mol。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.试写出下列反应的离子方程式:
(1)CO2通入足量澄清石灰水中_____________________________________________;
(2)CuSO4溶液与Ba(OH)2溶液混合________________________________________。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其可能含有SO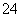 、Na+、CO
、Na+、CO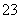 、H+、NO
、H+、NO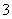 、HCO
、HCO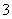 、Cl-等离子中的若干种。然后又作了如下分析,以确定这些离子是否大量存在。
、Cl-等离子中的若干种。然后又作了如下分析,以确定这些离子是否大量存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)原溶液中一定存在的离子是__________,一定不存在的离子是____________。
(2)在上述实验操作中,有错误的步骤是(填代号)______。对该错误改正的方法是(要作较详细的说明)__________________________________________________________________。
(3)到目前为止,不能肯定在原溶液中是否存在的离子是____________。
查看答案和解析>>
科目: 来源: 题型:
Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1∶16,则x的值为( )
A.5 B.4
C.3 D.2
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是( )
A.氨气通入醋酸溶液:CH3COOH+NH3===CH3COONH4
B.澄清的石灰水与盐酸反应:H++OH-===H2O
C.碳酸钡加入稀硫酸:BaCO3+2H+===Ba2++H2O+CO2↑
D.碳酸钙与盐酸反应:CO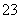 +2H+===H2O+CO2↑
+2H+===H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com