
科目: 来源: 题型:
据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)===SiO2(s) ΔH=-989.2 kJ·mol-1,有关键能数据如下表:
| 化学键 | Si—O | O===O | Si—Si |
| 键能/kJ·mol-1 | x | 498.8 | 176 |
则x的值为____________。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把________能转化为________能的装置。
(3)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是________(填字母序号)。
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(4)工业制备纯硅的反应为2H2(g)+SiCl4(g)===Si(s)+4HCl(g) ΔH=240.4 kJ·mol-1,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液中恰好完全反应,则反应过程中________(填“吸收”或“释放”)的热量为________kJ。
查看答案和解析>>
科目: 来源: 题型:
接触法制硫酸工艺中,其主反应在450 ℃并有催化剂存在下进行:2SO2(g)+O2(g)2SO3(g) ΔH=-190 kJ·mol-1。
(1)该热化学反应方程式的意义是________________________________________。
(2)已知单质硫16 g燃烧放热为149 kJ,写出硫燃烧的热化学方程式:________________________________________________________________________。
(3)由S(s)生成3 mol SO3(g)的ΔH=___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知胆矾溶于水时溶液温度降低。胆矾分解的热化学方程式为CuSO4·5H2O(s)===CuSO4(s)+5H2O(l)
ΔH=Q1 kJ·mol-1,室温下,若将1 mol无水硫酸铜溶解为溶液时放热Q2 kJ,则( )
A.Q1>Q2 B.Q1=Q2
C.Q1<Q2 D.无法比较
查看答案和解析>>
科目: 来源: 题型:
.S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O2(g)===SO2(g)
ΔH1=-297.16 kJ·mol-1
②S(正交,s)+O2(g)===SO2(g)
ΔH2=-296.83 kJ·mol-1
③S(单斜,s)===S(正交,s) ΔH3
下列说法正确的是( )
A.ΔH3=0.33 kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜,s)===S(正交,s) ΔH3<0,正交硫比单斜硫稳定
D.S(单斜,s)===S(正交,s) ΔH3>0,单斜硫比正交硫稳定
查看答案和解析>>
科目: 来源: 题型:
已知H2(g)、C2H4(g)和C2H5OH(l)的标准燃烧热分别是285.8 kJ·mol-1、1 411.0 kJ·mol-1和1 366.8 kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
A.-44.2 kJ·mol-1
B.44.2 kJ·mol-1
C.-330 kJ·mol-1
D.330 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式正确的是( )
A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)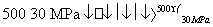 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C.已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+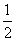 O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知充分燃烧a g乙炔气体时生成 1 mol 二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)
ΔH=-2b kJ·mol-1
B.C2H2(g)+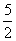 O2(g)===2CO2(g)+H2O(l)
O2(g)===2CO2(g)+H2O(l)
ΔH=2b kJ·mol-1
C.2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)
ΔH=-4b kJ·mol-1
D.2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)
ΔH=b kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知在1.01×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ的热量,下列热化学方程式正确的是( )
A.H2O(g)===H2(g)+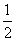 O2(g)
O2(g)
ΔH=242 kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l)
ΔH=-484 kJ·mol-1
C.H2(g)+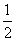 O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=242 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g)
ΔH=484 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
已知反应热:
①25 ℃、101 kPa时,2C(s)+O2(g)===2CO(g)
ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1
弱电解质电离时需吸热。下列结论正确的是( )
A.C的标准燃烧热大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目: 来源: 题型:
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的标准燃烧热为285.8 kJ·mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(l)
ΔH=-285.8 kJ·mol-1
C.Ba(OH)2·8H2O(s)+2NH4Cl(s)===BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0
D.已知中和热为57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com