
科目: 来源: 题型:
若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定能大量共存的离子组是( )
A.Al3+、Na+、NO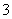 、Cl-
、Cl-
B.K+、Na+、Cl-、NO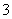
C.K+、Na+、Cl-、HCO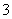
D.K+、Fe2+、SO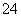 、NO
、NO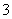
查看答案和解析>>
科目: 来源: 题型:
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________ (填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2===A+NH3↑,则生成物A的化学式为________,H2O2被称为“绿色氧化剂”的理由是_________________________________________。
(3)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数约为________。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是__________________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
查看答案和解析>>
科目: 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型消毒剂,工业上制备高铁酸钠有下列四种方法:
a.2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3NaCl+5H2O;
b.2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑;
c.Fe2O3+3Na2O2===2Na2FeO4+Na2O;
d.Fe(NO3)3+NaOH+Cl2―→Na2FeO4+NaNO3+NaCl+H2O。
请回答下列问题:
(1)下列判断正确的是________(填序号)。
A.方法a、b、c都可在水溶液中进行
B.根据a、b可知NaClO、Na2O2的氧化性均强于Na2FeO4的
C.FeSO4只有还原性,没有氧化性
D.能用KSCN溶液检验b的产物中是否含有FeSO4
(2)对于方法c下列说法正确的是________(填序号)。
A.Na2O2既是氧化剂又是还原剂
B.还原产物只有Na2O
C.3 mol Na2O2发生反应,有6 mol电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
(3)对于方法d,请回答下列问题:
①氧化剂与还原剂的物质的量之比为________。
②写出Na2FeO4与H2O反应的离子方程式:____________________________,
请你推测Na2FeO4除了能消毒杀菌外,另一个用途是____________________。
查看答案和解析>>
科目: 来源: 题型:
高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
MnO +3e-+2H2O===MnO2↓+4OH-
+3e-+2H2O===MnO2↓+4OH-
MnO +e-===MnO
+e-===MnO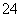 (溶液呈绿色)
(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的________影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为________________________________________________________。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________(填序号)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
查看答案和解析>>
科目: 来源: 题型:
根据表中信息判断,下列选项正确的是 ( )。
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO | Cl2、Mn2+…… |
A.第①组反应的其余产物为H2O
B.第②组反应中Cl2与FeBr2的物质的量之比小于或等于1∶2
C.第③组反应中生成1 mol Cl2,转移电子5 mol
D.氧化性由强到弱的顺序为MnO >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
查看答案和解析>>
科目: 来源: 题型:
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol。下列说法正确的是 ( )。
A.反应中硫元素被氧化,所有铁元素均被还原
B.氧化剂是Fe3+,氧化产物是Cu2+
C.反应中转移电子的物质的量为x mol
D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol
查看答案和解析>>
科目: 来源: 题型:
锑(Sb)在自然界一般以硫化物的形式存在。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
2Sb2S3+3O2+6Fe===Sb4O6+6FeS ①
Sb4O6+6C===4Sb+6CO ②
关于反应①、反应②的说法正确的是 ( )。
A.反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成1 mol Sb时,反应①与反应②中氧化剂的物质的量之比为1∶3
查看答案和解析>>
科目: 来源: 题型:
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO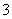 、Fe2+、NH
、Fe2+、NH 、H+、H2O,下列叙述正确的是 ( )。
、H+、H2O,下列叙述正确的是 ( )。
A.该反应说明Fe(NO3)2溶液不宜加酸酸化
B.该反应中氧化剂与还原剂物质的量之比为8∶1
C.若有1 mol NO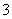 发生氧化反应,转移电子5 mol
发生氧化反应,转移电子5 mol
D.若将该反应设计成原电池,则负极反应为Fe3++e-===Fe2+
查看答案和解析>>
科目: 来源: 题型:
PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3∶2。则剩余固体的组成及物质的量之比是 ( )。
A.1∶1混合的Pb3O4、PbO
B.1∶2混合的PbO2、Pb3O4
C.1∶4∶1混合的PbO2、Pb3O4、PbO
D.1∶4∶1混合的PbO2、Pb3O4、PbO
查看答案和解析>>
科目: 来源: 题型:
把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平):
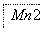 ……
……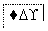
图1
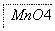
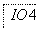
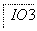
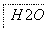

图2
对于该离子方程式的说法不正确的是 ( )。
A.IO 作氧化剂
作氧化剂
B.氧化性:Mn2+>IO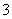
C.氧化剂与还原剂的物质的量之比为5∶2
D.若有2 mol Mn2+参加反应时,则转移10 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com