
科目: 来源: 题型:
已知离子方程式:As2S3+H2O+NO ―→AsO
―→AsO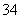 +SO
+SO +NO↑+________(未配平),下列说法错误的是 ( )。
+NO↑+________(未配平),下列说法错误的是 ( )。
A.配平后水的化学计量数为4
B.反应后溶液呈酸性
C.配平后氧化剂与还原剂的物质的量之比为3∶28
D.氧化产物为AsO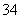 和SO
和SO
查看答案和解析>>
科目: 来源: 题型:
一未配平的离子方程式为______+XO +6H+===3X2+3H2O,据此判断,氧化产物和还原产物的物质的量之比为 ( )。
+6H+===3X2+3H2O,据此判断,氧化产物和还原产物的物质的量之比为 ( )。
A.1∶1 B.3∶1
C.5∶1 D.7∶1
查看答案和解析>>
科目: 来源: 题型:
(NH4)2PtCl6晶体受热分解,生成氮气、氯化氢、氯化铵和金属铂,在此分解反应中,氧化产物与还原产物的物质的量之比是 ( )。
A.2∶3 B.3∶2
C.4∶3 D.1∶3
查看答案和解析>>
科目: 来源: 题型:
下列有关反应SiO2+3C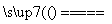 SiC+2CO↑的叙述中,正确的是 ( )。
SiC+2CO↑的叙述中,正确的是 ( )。
A.氧化剂是SiO2
B.氧化剂与还原剂的物质的量之比为1∶2
C.碳在反应中只作还原剂
D.若生成1 mol SiC,则转移电子2 mol
查看答案和解析>>
科目: 来源: 题型:
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
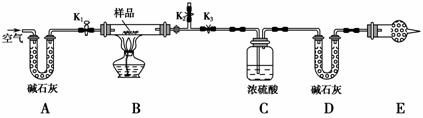
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是____________________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是______________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________________________________________
____________________________________________________、
___________________________________________________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是______________________ _______________________________________________________。
②E处干燥管中盛放的药品是________,其作用是___________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量分数________(填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
烧碱、纯碱等都是重要的化工原料。
(1)利用如图装置可以证明二氧化碳与烧碱溶液发生了反应。

①若将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是_______________________________________________。
②若其他操作不变,将A与C连接,可观察到的现象是______________________________________________。
(2)向100 mL 1 mol·L-1烧碱溶液中通入一定量CO2充分反应后,将溶液在低温下蒸干得到白色固体X,X的组成可能有四种情况,按出现的先后顺序分别是Ⅰ.NaOH、Na2CO3,Ⅱ.__________________,Ⅲ.Na2CO3、NaHCO3,Ⅳ.__________________________________________。
①常温下,将得到的固体X重新溶于水,在所得溶液中加入盐酸,使溶液的pH=7,再将溶液蒸干,得到固体的质量为________ g。
②若要验证白色固体X是第Ⅰ种组成,依次加入的试剂为________(填字母序号)。
a.盐酸 b.MgCl2溶液
c.BaCl2溶液 d.Ba(OH)2溶液
在验证的过程中,一定需要进行的操作是________(填字母序号)。
a.萃取 b.洗涤
c.过滤 d.分馏
③若白色固体X为第Ⅲ种组成,下列实验方案中不能测定其中NaHCO3质量分数的是________(填字母序号)。
a.取m g X与足量Ba(OH)2溶液充分反应,过滤,洗涤,烘干得n g固体
b.取m g X与足量盐酸充分反应,加热,蒸干,灼烧得n g固体
c.取m g X充分加热,减重n g
d.取m g X与足量稀硫酸充分反应,逸出的气体被足量碱石灰吸收,增重n g
④若白色固体X的质量为7.0 g,则X的组成为________(填“Ⅰ”、“Ⅱ”、“Ⅲ”或“Ⅳ”)。
查看答案和解析>>
科目: 来源: 题型:
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取可以通过如下反应完成:Na+NaNO3 Na2O+N2↑(未配平)。请回答下列问题:
Na2O+N2↑(未配平)。请回答下列问题:
(1)上述反应的氧化剂是________(写化学式)。制取Na2O时,若金属钠与NaNO3按质量比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的Na2O的质量为________ kg。
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。

可选用的试剂:
a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液
e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字母表示) | 实验需直接测定的有关物理量(用文字说明) |
(3)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下:

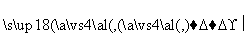



该Na2O产品中Na2O的质量分数为________。
查看答案和解析>>
科目: 来源: 题型:
一化学研究性学习小组对某Na2CO3和NaHCO3混合溶液的组成进行探究。取20.0 mL该混合溶液不断加入1.00 mol·L-1的稀盐酸,加入盐酸的体积和产生的现象见下表。
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现象 | 无气体 | 产生气体 | 无气体 |
则混合溶液中c(HCO )为 ( )。
)为 ( )。
A.1.00 mol·L-1 B.0.50 mol·L-1
C.1.50 mol·L-1 D.2.00 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
下列事实及其解释不正确的是 ( )。
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
查看答案和解析>>
科目: 来源: 题型:
120 mL含有0.20 mol碳酸钠的溶液和200 mL 盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是 ( )。
A.2.0 mol·L-1 B.1.5 mol·L-1
C.0.18 mol·L-1 D.0.24 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com