
科目: 来源: 题型:
Ⅰ.2008年5月12日汶川大地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上制取漂白粉的化学方程式为______________________________________。
(2)漂白粉的有效成分是(填化学式)_______________________________。
(3)漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸。化学反应方程式为________________________________________________________________________
________________________________________________________________________。
Ⅱ.钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术。其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃。其过程可以用如下方程式表示:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O===3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
则反应②中的氧化剂是________(填化学式),整个过程中,每有168 g Fe参加反应,则转移________ mol 电子。
查看答案和解析>>
科目: 来源: 题型:
SO2被称为“空中死神”,其对环境的危害常表现为__________________。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。
(1)工业上常用生石灰来处理煤炭中的SO2,这是利用了SO2属于__________氧化物的性质。
(2)近年来,有人提出了一种利用电解饱和氯化钠溶液(2NaCl+2H2O===2NaOH+Cl2+H2)循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
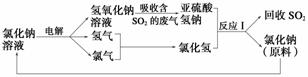
①此种方法中,可以循环利用的物质是_____________________________________。
②写出反应Ⅰ的离子方程式:_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是中学常见的混合物分离或提纯的基本装置。
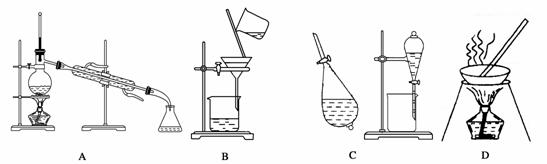
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3__________________________________________;
(2)从碘水中提取碘__________________________________________;
(3)用自来水制取蒸馏水___________________________________;
(4)分离植物油和水_______________________________________;
(5)除去粗盐中的泥沙__________________________________________;
(6)与海水晒盐原理相符的是__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
向含有a mol AlCl3的溶液中加入含b mol KOH的溶液,生成沉淀的物质的量可能是( )
①a mol ②b mol ③ mol ④
mol ④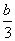 mol ⑤0 mol ⑥(4a-b)mol
mol ⑤0 mol ⑥(4a-b)mol
A.①②④⑤⑥ B.①④⑤⑥ C.①②③⑤⑥ D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
已知浓H2SO4和Fe3+都可以将Cu氧化成Cu2+,浓H2SO4也可以将Br-氧化成Br2,Fe与Br2反应生成FeBr3.由此可以确定上述有关物质氧化性由强到弱的顺序为( )
A.浓H2SO4>Br2>Fe3+>Cu2+ B.浓H2SO4>Cu2+>Fe3+>Br2
C.Br2>浓H2SO4>Fe3+>Cu2+ D.Fe3+>Cu2+>Br2>浓H2SO4
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是( )
A.碳酸钡与盐酸反应:2H++BaCO3===Ba2++H2O+CO2↑
B.氢氧化钡溶液与稀硫酸混合:Ba2++SO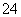 +H++OH-===BaSO4↓+H2O
+H++OH-===BaSO4↓+H2O
C.氯气通入蒸馏水:Cl2+H2O===Cl-+ClO-+2H+
D.CO2通入过量的澄清石灰水中:CO2+Ca(OH)2===CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
向某HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如下图所示,则原稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比为( )
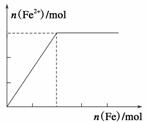
A.4∶1 B.3∶1 C.2∶1 D.1∶1
查看答案和解析>>
科目: 来源: 题型:
被称为万能还原剂的NaBH4(NaBH4中H为-1价)能溶于水并和水反应,NaBH4+2H2O===NaBO2+4H2↑,下列有关该反应的说法中,正确的是( )
A.NaBH4既是氧化剂又是还原剂 B.NaBH4是氧化剂,H2O是还原剂
C.硼元素被氧化,氢元素被还原 D.被氧化的元素与被还原的元素质量比为1∶1
查看答案和解析>>
科目: 来源: 题型:
用98%的浓硫酸(密度为1.84 g·cm-3)配制100 mL 1 mol·L-1的稀硫酸,现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒
按使用仪器的先后顺序排列正确的是( )
A.④③⑦⑤⑥ B.②⑤⑦⑥ C.①③⑤⑥⑦ D.②⑥③⑦⑤⑥
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol N2所含有的原子数为NA
B.标准状况下,16 g NH3中含有的分子数为NA
C.标准状况下,22.4 L氯化氢所含的原子数为NA
D.500 mL 1.0 mol·L-1硫酸钠溶液中所含的钠离子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com