
科目: 来源: 题型:
如图是298 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )。
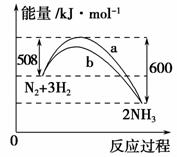
A.该反应的热化学方程式为N2+3H22NH3 ΔH=-92 kJ·mol-1
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热发生改变
D.温度、体积一定,1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
查看答案和解析>>
科目: 来源: 题型:
肼(H2N—NH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol 化学键所需的能量(kJ):N≡N 为942、O=O为500、N—N为154,则断裂1 mol N—H 键所需的能量(kJ)是 ( )。

A.194 B.391
C.516 D.685
查看答案和解析>>
科目: 来源: 题型:
已知在1×105Pa、298 K条件下,2 mol H2 燃烧生成水蒸气放出 484 kJ热量,下列热化学方程式正确的是 ( )。
A.H2O(g)===H2 (g) +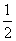 O2(g)
O2(g)
ΔH=+242 kJ·mol-1
B.2H2 (g)+O2 (g) ===2H2O(l)
ΔH=-484 kJ·mol-1
C.H2(g)+1/2O2 (g)===H2O(g)
ΔH=+242 kJ·mol-1
D.2H2(g)+O2 (g) ===2H2O (g)
ΔH=+484 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
如图所示,下列说法不正确的是 ( )。

A.反应过程(1)的热化学方程式为 A2 (g)+B2(g)===C(g) ΔH1=-Q kJ·mol-1
B.反应过程(2)的热化学方程式为C(g)===A2(g)+B2(g) ΔH2=+Q1 kJ·mol-1
C.Q与Q1的关系:Q>Q1
D.ΔH2>ΔH1
查看答案和解析>>
科目: 来源: 题型:
某反应由两步反应 A BC构成,反应过程中的能量变化曲线如图,下列叙述正确的是 ( )。

A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.加入催化剂会改变反应的焓变
D.整个反应的ΔH=E1-E2
查看答案和解析>>
科目: 来源: 题型:
下列反应类型中可以吸收能量的反应是 ( )。
①化合反应 ②分解反应 ③置换反应 ④复分解反应
⑤氧化还原反应
A.①②③④⑤ B.②④
C.①③④⑤ D.②
查看答案和解析>>
科目: 来源: 题型:
工业上由 CO2 和 H2 合成气态甲醇的热化学方程式为:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH=-50 kJ·mol-1。下面表示合成甲醇的反应的能量变化示意图,其中正确的是 ( )。
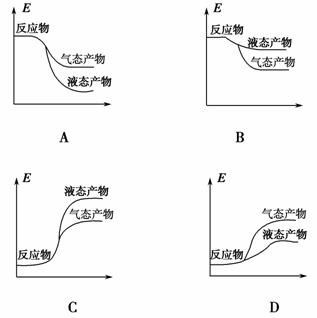
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是 ( )。
A.化学变化过程是原子的重新组合过程
B.根据化学反应中的能量变化情况,化学反应可分为吸热反应和放热反应
C.化学反应中的能量变化多少与其反应物用量有关
D.化学反应中的能量变化都是以热能形式表现出来的
查看答案和解析>>
科目: 来源: 题型:
火力发电厂释放出大量二氧化碳,对燃煤废气进行脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。将CO2转化为甲醇是一种新型脱碳技术,其反应为CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH。
(1)取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图Ⅰ所示,则上述CO2转化为甲醇的反应的ΔH________0(填“>”、“<”或“=”)。
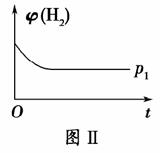

(2)如图Ⅱ是在恒温密闭容器中,压强为p1时H2的体积分数随时间t的变化曲线,请在图中画出该反应在p2(p2>p1)时H2的 体积分数随时间t的变化曲线。
(3)在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的物质的量浓度随时间的变化如图Ⅲ所示。

则0~10 min内,氢气的平均反应速率为________;该温度下,反应的平衡常数为________(保留三位有效数字);10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
反应A(g)B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
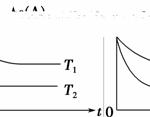
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”、“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______________________________________。
②反应的平衡常数K=________________________________________。
③反应在0~5 min区间的平均反应速率v(A)=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com