
科目: 来源: 题型:
已知H2(g)+Cl2(g)===2HCl(g) ΔH=-184.6 kJ·mol-1,则反应:HCl(g)===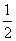 H2(g)+
H2(g)+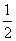 Cl2(g)的ΔH为 ( )。
Cl2(g)的ΔH为 ( )。
A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1
C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
某同学发现在炽热的煤炭上洒少量水,煤炉中会产生淡蓝色的火焰,炉火更旺。因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧时放出更多的热量”。已知:煤炭的燃烧热为 393.15 kJ · mol-1 ,氢气的燃烧热为 242 kJ· mol-1 ,一氧化碳的燃烧热为 283 kJ · mol-1 。下列有关说法正确的是
A.表示氢气燃烧热的热化学方程式为 2H2(g)+ O2(g)===2H2O (l) ΔH= -242 kJ · mol-1
B.表示CO 燃烧热的热化学方程式为 2CO(g)+ O2(g)===2CO2 (g) ΔH= - 566 kJ · mol-1
C.“炉火更旺”是因为少量的固体煤炭转化为可燃性气体
D.因 242 kJ·mol-1 +283 kJ· mol-1 >393.15 kJ·mol-1 ,故该同学的结论是对的
查看答案和解析>>
科目: 来源: 题型:
分别向1 L 0.5 mol·L-1的Ba(OH)2溶液中加入①浓硫酸、②稀硫酸、③稀硝酸,恰好完全反应时的热效应分别为ΔH1、ΔH2、ΔH3,下列关系中正确的是 ( )。
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH2<ΔH3
C.ΔH1>ΔH2=ΔH3 D.ΔH1=ΔH2<ΔH3
查看答案和解析>>
科目: 来源: 题型:
已知反应:①101 kPa时,2C(s)+O2(g)===2CO(g)
ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1
下列结论正确的是 ( )。
A.碳的燃烧热的数值大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀硫酸与稀Ba(OH)2溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目: 来源: 题型:
为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是 ( )。
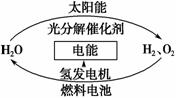
A.H2O的分解反应是放热反应
B.氢能源已被普遍使用
C.2 mol H2O具有的总能量低于2 mol H2和1 mol O2的能量
D.氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
科目: 来源: 题型:
白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
(1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为P4(s,白磷)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1
P(s,红磷)+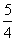 O2(g)===
O2(g)===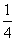 P4O10(s) ΔH2=-738.5 kJ·mol-1
P4O10(s) ΔH2=-738.5 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为_______________________
_______________________________________________________________。
(2)已知298 K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)===P4O6(s)
ΔH=-1 638 kJ·mol-1。在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________,反应过程中放出的热量为________。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P 198,Cl—Cl 243,P—Cl 331。则反应P4(s,白磷)+6Cl2(g)===4PCl3(s)的反应热
ΔH=________。

查看答案和解析>>
科目: 来源: 题型:
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程中的能量关系可用右图简单表示(图中的ΔH表示生成
1 mol产物的数据)。

(1)写出表示S8燃烧热的热化学方程式________________________________
________________________________________________________________。
(2)写出SO3分解生成SO2和O2的热化学方程式_________________________
_________________________________________________________________。
(3)若已知1个S8分子中有8个硫硫键,硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,则S8分子中硫硫键的键能为____________。
查看答案和解析>>
科目: 来源: 题型:
图像法是研究化学反应的焓变的一种常用方法。

图1
(1)已知化学反应A2(g)+B2(g)===2AB(g)的能量变化曲线如图1所示,判断下列叙述中正确的是________。
A.每生成2 mol AB时吸收 b kJ 热量
B.该反应热ΔH=+(a-b) kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键时放出a kJ能量
(2)在微生物作用的条件下,NH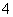 经过两步反应被氧化成NO
经过两步反应被氧化成NO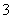 。两步反应的能量变化如图2所示:
。两步反应的能量变化如图2所示:
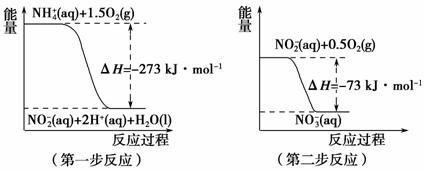
图2
1 mol NH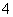 (aq)全部氧化成NO
(aq)全部氧化成NO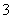 (aq)的热化学方程式是____________________________________________。
(aq)的热化学方程式是____________________________________________。
(3)图3中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素。
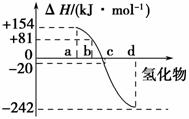
图3
①非金属元素氢化物的稳定性与氢化物生成热ΔH的关系为_______________________________________________________________。
②写出硒化氢发生分解反应的热化学方程式____________________________
_______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
化学反应的本质是旧化学键的断裂和新化学键的形成。已知某些化学键的键能数据如下:
| 化学键 | H—H | Cl—Cl | H—Cl |
| 键能/(kJ·mol-1) | 436 | 243 | 431 |
则下列热化学方程式不正确的是 ( )。
A.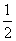 H2(g)+
H2(g)+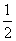 Cl2(g)===HCl (g)
Cl2(g)===HCl (g)
ΔH=-91.5 kJ· mol -1
B.H2 (g) +Cl2 (g) ===2HCl (g)
ΔH=-183 kJ· mol-1
C.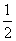 H2(g)+
H2(g)+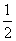 Cl2(g)===HCl (g)
Cl2(g)===HCl (g)
ΔH=+91.5 kJ· mol -1
D.2HCl (g) ===H2 (g)+Cl2 (g)
ΔH=+183 kJ· mol-1
查看答案和解析>>
科目: 来源: 题型:
在298K、1.01×105Pa下,将32 g SO2通入750 mL 1 mol·L-1 KOH溶液中充分反应。测得反应放出x kJ的热量。已知在该条件下,1 mol SO2通入1 L 2 mol ·L-1KOH溶液中充分反应放出y kJ的热量。则 SO2与KOH溶液反应生成 KHSO3的热化学方程式正确的是 ( )。
A.SO2(g)+KOH (aq)===KHSO3 (aq)
ΔH=-(4x-y) kJ·mol
B.SO2(g)+KOH (aq)===KHSO3 (aq)
ΔH=-(2x-y) kJ·mol-1
C.SO2(g)+KOH (aq)===KHSO3 (aq)
ΔH=-(2y-x) kJ·mol
D.2SO2(g)+2KOH (l)===2KHSO3 (l)
ΔH=-(8x-2y) kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com